Ung thư tuyến giáp là bệnh lý ác tính nội tiết hay gặp nhất, chiếm khoảng 2% tổng số các loại ung thư. PGS.TS Nguyễn Nghiêm Luật - Bệnh viện Đa khoa MEDLATEC đã có bài nghiên cứu về các dấu ấn sinh học huyết thanh, các dấu ấn sinh học sinh thiết lỏng, các thay đổi phân tử và điều trị đích ung thư tuyến giáp. Kính mời các bác sĩ đồng nghiệp cùng người dân trên cả nước cùng tham khảo bài viết sau!
30/01/2023 | Bệnh ung thư tuyến giáp và những thông tin cần biết 30/01/2023 | Ung thư tuyến giáp thể nhú là bệnh gì? 29/12/2022 | Ung thư tuyến giáp có nguy hiểm không và cách phòng ngừa 27/12/2022 | Triệu chứng ung thư tuyến giáp cần nhận biết sớm!
PGS TS Nguyễn Nghiêm Luật
Bệnh viện Đa khoa MEDLATEC
Tóm tắt
Ung thư tuyến giáp (TC) là bệnh lý ác tính nội tiết hay gặp nhất, chiếm khoảng 2% tổng số các loại ung thư. Có 5 loại ung thư tuyến giáp chính: (1) Ung thư biểu mô tuyến giáp thể nhú (PTC, 80%), (2) ung thư biểu mô tuyến giáp thể nang (FTC, 10%), (3) ung thư tế bào Hürthle (2%-3%), (4) ung thư biểu mô tuyến giáp thể tủy (MTC, 2%-4%) và (5) ung thư biểu mô tuyến giáp thể không biệt hóa (ATC, 1%-2%).
1) Nguyên nhân và các yếu tố nguy cơ: Ung thư tuyến giáp có liên quan đến một số bệnh di truyền, nhưng nguyên nhân chính xác của hầu hết các ung thư tuyến giáp hiện vẫn chưa được biết. Các yếu tố nguy cơ ung thư tuyến giáp không thể thay đổi gồm: Giới tính và tuổi tác, tình trạng di truyền, … Các yếu tố nguy cơ ung thư tuyến giáp có thể thay đổi gồm: Bức xạ, thừa cân hoặc béo phì, chế độ ăn nhiều iốt có thể làm tăng nguy cơ ung thư tuyến giáp thể nhú, trong khi chế độ ăn kiêng iốt thấp có thể làm tăng nguy cơ ung thư tuyến giáp thể nang.
2) Các dấu hiệu và triệu chứng: Ung thư tuyến giáp có thể gây ra bất kỳ dấu hiệu hoặc triệu chứng nào sau đây: Có một khối u ở cổ, đôi khi phát triển nhanh chóng, sưng ở cổ, đau ở phía trước cổ, đôi khi đau lên đến tai, khàn giọng hoặc những thay đổi khác về giọng nói không biến mất, khó nuốt, khó thở và ho liên tục nhưng không phải do cảm lạnh.
3) Các dấu ấn sinh học huyết thanh: Một số xét nghiệm huyết thanh có thể được thực hiện trong quá trình chẩn đoán và theo dõi bệnh nhân trong và sau khi điều trị có thể gồm: Hormone kích thích tuyến giáp (TSH), các nồng độ hormone tuyến giáp như hormone tuyến giáp triiodothyronine (T3) và thyroxine (T4), thyroglobulin (Tg), kháng thể thyroglobulin (TgAb). Các xét nghiệm đặc hiệu cho ung thư tuyến giáp thể tủy có thể gồm calcitonin, kháng nguyên carcinoembryonic (CEA) và procalcitonin (PCT).
4) Các dấu ấn sinh học dựa trên sinh thiết lỏng: Các dấu ấn sinh học dựa trên sinh thiết lỏng được sử dụng để xác định chẩn đoán bệnh nhân, dự đoán tiên lượng và theo dõi sự tái phát của khối u hoặc đáp ứng điều trị, có thể bao gồm: các tế bào khối u lưu thông (CTCs), các DNA tự do lưu thông (cfDNA), các miRNA và túi ngoại bào (EVs) có nguồn gốc từ khối u.
5) Các thay đổi phân tử và điều trị đích: Các con đường tín hiệu chủ yếu trong ung thư tuyến giáp là con đường MAPK và PI3K/AKT. Các thuốc điều trị đích ung thư tuyến giáp thể nhú hoặc thể nang có thể gồm: Các thuốc ức chế multikinase (lenvatinib, sorafenib và cabozantinib), thuốc ức chế RET (selpercatinib) và các thuốc ức chế TRK (larotrectinib và entrectinib); các thuốc điều trị đích ung thư tuyến giáp thể tủy có thể gồm: Các thuốc ức chế Multikinase (vandetanib và cabozantinib), các thuốc ức chế RET (selpercatinib và pralsetinib); các thuốc điều trị đích ung thư tuyến giáp thể không biệt hóa có thể gồm: các thuốc ức chế BRAF và MEK (dabrafenib và trametinib), thuốc ức chế RET (selpercatinib) và các thuốc ức chế TRK (larotrectinib và entrectinib).
Thyroid Cancer: Serum Biomarkers, Liquid Biopsy-based Biomarkers, Molecular Alterations and Targeted Therapy
Luat Nghiem Nguyen
MEDLATEC General Hospital
Abstract
Thyroid cancer (TC) is the most frequent endocrine malignancy, accounting for about 2% of total cancers. There are 5 main types of thyroid cancer: (1) Papillary thyroid carcinoma (PTC, 80%), (2) follicular thyroid carcinoma (FTC, 10%), (3) Hürthle cell cancer (2%-3%), (4) medullary thyroid carcinoma (MTC, 2%-4%), and (5) anaplastic thyroid carcinoma (ATC, 2%).
1) Causes and risk factors. Thyroid cancer is linked with a number of inherited conditions, but the exact cause of most thyroid cancers is not yet known. Risk factors that can't be changed include: Gender and age, hereditary conditions, … Risk factors that may be changed include: Radiation, being overweight or obese, a diet high in iodine may increase the risk of papillary thyroid cancer, while a diet low in iodine may increase the risk of follicular thyroid cancers.
2) Signals and symptoms. Thyroid cancer can cause any of the following signs or symptoms: A lump in the neck, sometimes growing quickly, swelling in the neck, pain in the front of the neck, sometimes going up to the ears, hoarseness or other voice changes that do not go away, trouble swallowing, trouble breathing and a constant cough that is not due to a cold.
3) Serum biomarkers. Some serum tests may be done during diagnosis and to monitor the patient during and after treatment include: Thyroid-stimulating hormone (TSH), thyroid hormone levels such as thyroid hormones triiodothyronine (T3) and thyroxine (T4), thyroglobulin (Tg), thyroglobulin antibodies (TgAb). Medullary type-specific tests may include: calcitonin and carcinoembryonic antigen (CEA) and procalcitonin (PCT).
4) Liquid biopsy-based biomarkers. Liquid biopsy-based biomarkers use to define a patient's diagnosis, estimate their prognosis, and monitor tumor recurrence or treatment response, may include: circulating tumor cells (CTCs), circulating free DNA (cfDNA), miRNAs, and tumor-derived extracellular vesicles (EVs).
5) Molecular alterations and targeted therapy. Key signaling pathways in thyroid cancer are the MAPK and PI3K/AKT pathways. Targeted drugs for papillary or follicular thyroid cancer may include: Multikinase inhibitors (lenvatinib, sorafenib, and cabozantinib), RET inhibitors (selpercatinib), and TRK inhibitors (larotrectinib and entrectinib); targeted drugs for medullary thyroid cancer may include: Multikinase inhibitors (vandetanib and cabozantinib), RET inhibitors (selpercatinib and pralsetinib); targeted drugs for anaplastic thyroid cancer may include: BRAF and MEK inhibitors (dabrafenib and trametinib), RET inhibitors (selpercatinib), and TRK inhibitors (larotrectinib and entrectinib).
******
Ung thư tuyến giáp là sự phát triển không kiểm soát của các tế bào tuyến giáp. Khoảng 90% nhân giáp hay khối u tuyến giáp là lành tính.
Tỷ lệ chẩn đoán ung thư tuyến giáp đã tăng lên trên toàn thế giới trong thập kỷ qua, có thể là do các công nghệ phát hiện nhạy hơn. Số các ung thư tuyến giáp trên thế giới năm 2022 là 43.800 ca, chiếm 2,3 % số ca các ung thư mới, với số ca tử vong là 2.230, chiếm 0,4% số ca các ung thư và hầu hết các ung thư tuyến giáp đều có tiên lượng tốt và có thể chữa khỏi, nếu chúng chưa di căn sang các vùng khác của cơ thể, tỷ lệ sống sót 5 năm (2012-2018) là 98,4% [9].
Dựa trên khả năng biệt hóa của tế bào, các ung thư tuyến giáp có thể thuộc loại biệt hóa (differentiated) như ung thư thể nhú (papillary), thể nang (follicular) hoặc tế bào Hürthle, ung thư thể tủy (medullary) và ung thư thể không biệt hóa (anaplastic).
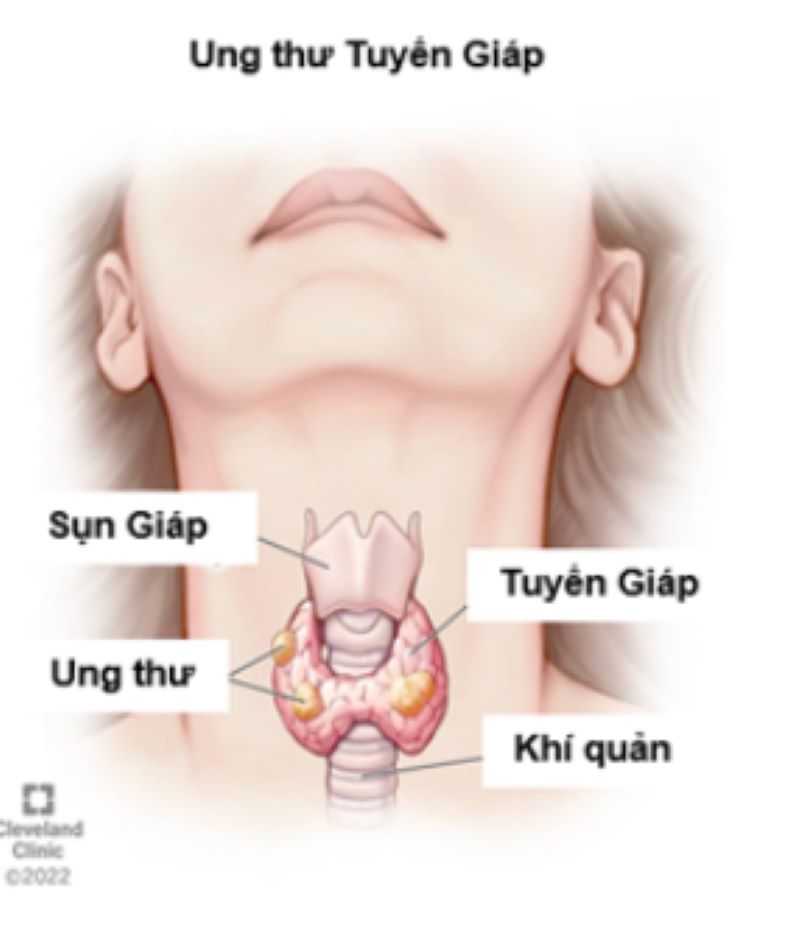
Hình 1. Ung thư Tuyến Giáp (nguồn: Cleveland Clinic, 2022)
Ung thư tuyến giáp có thể được phân thành 5 loại chủ yếu, bao gồm:
1) Ung thư biểu mô tuyến giáp thể nhú (papillary thyroid carcinoma: PTC), là ung thư tuyến giáp phổ biến nhất, chiếm khoảng 80%, phát triển chậm và hiếm khi gây tử vong.
2) Ung thư biểu mô tuyến giáp thể nang (follicular thyroid carcinoma: FTC), còn gọi là ung thư biểu mô tuyến tuyến giáp thể nang (follicular thyroid adenocarcinoma), là ung thư tuyến giáp phổ biến thứ hai, chiếm khoảng 10%, hay gặp ở các vùng chế độ ăn thiếu i-ốt.
3) Ung thư biểu mô tế bào Hürthle (Hürthle cell carcinoma), còn được gọi là ung thư biểu mô tế bào ưa oxy (oxyphil cell carcinoma), cũng là một dạng ung thư biểu mô tuyến giáp thể nang, chiếm khoảng 2-3% số ca ung thư tuyến giáp, khó phát hiện và điều trị hơn.
4) Ung thư biểu mô tuyến giáp thể tủy (medullary thyroid carcinoma: MTC): chiếm 4% các loại ung thư tuyến giáp. MTC có thể tự phát hoặc do di truyền. Ung thư tuyến giáp thể tủy di truyền là do đột biến gen RET và thường liên quan đến đa u nội tiết loại 2 (multiple endocrine neoplasia type 2: MEN), cũng có thể do đột biến gen RET. Ung thư này cần nhiều hơn một loại điều trị và khó chữa khỏi hơn các ung thư tuyến giáp phổ biến hơn.
5) Ung thư biểu mô tuyến giáp thể thể không biệt hóa (anaplastic thyroid carcinoma: ATC), chỉ chiếm 2% trong số các ca ung thư tuyến giáp, là loại ung thư tuyến giáp lây lan nhanh và khó điều trị nhất [1].
Ngoài ra còn có các u lympho nguyên phát (primary lymphomas), sarcoma và ung thư tuyến cận giáp (Parathyroid cancer), là các loại ung thư tuyến giáp rất hiếm gặp [1, 2].
Hầu hết các bệnh ung thư tuyến giáp hiện được phát hiện sớm, khi chúng có thể điều trị được. Ung thư tuyến giáp thể nhú và thể nang có tiên lượng tốt. Theo Hiệp hội Ung thư Hoa Kỳ, 97% bệnh nhân ung thư tuyến giáp sống sót sau 10 năm chẩn đoán.
Trong bài viết này, nguyên nhân và các yếu tố nguy cơ, các dấu hiệu và triệu chứng, các dấu ấn sinh học huyết thanh, các dấu ấn sinh học sinh thiết lỏng, các thay đổi phân tử và điều trị đích ung thư tuyến giáp sẽ được trình bày.
1. Nguyên nhân và các yếu tố nguy cơ của ung thư tuyến giáp
1.1. Nguyên nhân gây ung thư tuyến giáp
Ngươi ta thấy rằng ung thư tuyến giáp có liên quan đến một số tình trạng di truyền, tuy nhiên, nguyên nhân chính xác của hầu hết các ung thư tuyến giáp hiện chưa được biết [1].
1) Đối với ung thư tuyến giáp thể nhú. Một số đột biến DNA đã được thấy trong ung thư tuyến giáp thể nhú. Những thay đổi của gen RET, gọi là gen gây ung thư tuyến giáp thể nhú (PTC), được thấy ở khoảng 10% đến 30% trường hợp ung thư tuyến giáp thể nhú và tỷ lệ phần trăm lớn hơn ở trẻ em hoặc có liên quan đến phơi nhiễm phóng xạ. Ung thư tuyến giáp thể nhú cũng có thể có gen BRAF bị đột biến. Đột biến BRAF ít phổ biến hơn ở ung thư tuyến giáp ở trẻ em và ung thư do tiếp xúc với bức xạ. Rất hiếm ung thư tuyến giáp thể nhú có sự thay đổi ở cả hai gen RET và BRAF. Những thay đổi ở các gen khác cũng có thể liên quan đến ung thư tuyến giáp thể nhú, như ở gen NTRK1.
2) Đối với ung thư tuyến giáp thể nang. Các thay đổi mắc phải ở gen gây ung thư RAS cũng như sự sắp xếp lại gen PAX8-PPAR-γ có thể gây ra ung thư tuyến giáp thể nang.
3) Đối với ung thư tuyến giáp thể tủy. Người bị ung thư tuyến giáp thể tủy (MTC) cũng có thể có đột biến ở gen RET. Gần như tất cả các bệnh nhân bị thể MTC di truyền và khoảng 1/10 bệnh nhân bị thể MTC lẻ tẻ (không di truyền) có đột biến gen RET. Những người bị ung thư tuyến giáp thể tủy gia đình (familial MTC) và đa u tuyến nội tiết loại 2 (multiple endocrine neoplasia type 2: MEN 2) thừa hưởng đột biến gen RET từ cha hoặc mẹ.
4) Đối với ung thư tuyến giáp thể không biệt hóa. Ung thư tuyến giáp thể không biệt hóa có thể có một số đột biến trên và có các thay đổi ở gen ức chế khối u TP53 [1].
1.2. Các yếu tố nguy cơ ung thư tuyến giáp
1.2.1. Các yếu tố nguy cơ không thể thay đổi
1) Giới tính. Ung thư tuyến giáp (cũng như hầu hết các bệnh về tuyến giáp) xảy ra ở phụ nữ nhiều hơn khoảng 3 lần so với nam giới.
2) Độ tuổi. Ung thư tuyến giáp có thể xảy ra ở mọi lứa tuổi, nhưng nguy cơ mắc bệnh cao sớm hơn đối với phụ nữ (ở độ tuổi 40 hoặc 50) so với nam giới (ở độ tuổi 60 hoặc 70).
3) Tình trạng di truyền. Một số tình trạng di truyền cũng như tiền sử gia đình có thể có liên quan đến các loại ung thư tuyến giáp khác nhau, chẳng hạn như:
- Ung thư tuyến giáp thể tủy. Khoảng 2/10 số ca ung thư biểu mô tuyến giáp thể tủy (MTC) là do thừa hưởng một gen bất thường. Những trường hợp này được gọi là ung thư biểu mô tuyến giáp thể tủy gia đình (FMTC).
- Sự kết hợp giữa ung thư biểu mô tuyến giáp thể tủy gia đình (FMTC) và các khối u của các tuyến nội tiết khác được gọi là đa u tuyến nội tiết loại 2 (MEN 2). MEN 2 có 2 loại phụ là MEN 2a và MEN 2b, đều do đột biến ở gen RET gây ra.
Trong đa u tuyến nội tiết loại 2a (MEN 2a), ung thư biểu mô tuyến giáp thể tủy (MTC) xảy ra cùng với các khối u tủy thượng thận (pheochromocytomas) và với khối u tuyến cận giáp. Các khối u tủy thượng thận xảy ra khi có tình trạng quá sản các tế bào tủy thượng thận, rất hiếm gặp và đa phần lành tính. Các khối u tủy thượng thận sản xuất ra các catecholamine (adrenalin, noradrenalin, …) nhiều hơn bình thường và gây ra các triệu chứng như tim đập nhanh, nhức đầu và ra mồ hôi.
Trong đa u tuyến nội tiết loại 2b (MEN 2b), ung thư biểu mô tuyến giáp thể tủy (MTC) có liên quan đến u tế bào ưa crôm và sự phát triển lành tính của mô thần kinh trên lưỡi và những nơi khác được gọi là u thần kinh. Loại phụ này ít phổ biến hơn nhiều so với loại phụ MEN 2a.
Ở các thể ung thư biểu mô tuyến giáp thể tủy (MTC) di truyền này, ung thư thường phát triển ở tuổi trẻ và có thể lây lan sớm. Ung thư biểu mô tuyến giáp thể tủy (MTC) hoạt động mạnh nhất ở hội chứng MEN 2b. Nếu MEN 2a, MEN 2b hoặc FMTC đơn lẻ có ở gia đình một người, người đó có thể có nguy cơ bị MTC rất cao, cần được xét nghiệm di truyền.
- Các thư tuyến giáp khác. Những người bị một số bệnh di truyền nhất định có nguy cơ cao mắc các thể ung thư tuyến giáp phổ biến hơn. Tỷ lệ ung thư tuyến giáp cao hơn xảy ra ở những người có tình trạng di truyền không phổ biến như:
+ Đa polyp tuyến gia đình (FAP). Những người mắc hội chứng này phát triển nhiều polyp đại tràng và có nguy cơ ung thư đại tràng rất cao. Họ cũng có sự tăng nguy cơ bị một số ung thư khác, như ung thư tuyến giáp thể nhú. Hội chứng Gardner là một thể phụ của FAP, bệnh nhân có một số khối u lành tính. Cả hội chứng Gardner và FAP đều do sự khiếm khuyết gen APC gây ra.
+ Bệnh Cowden. Những người mắc hội chứng này có nguy cơ cao mắc các vấn đề về tuyến giáp và một số khối u lành tính (gồm một số khối u gọi là hamartomas). Họ cũng bị tăng nguy cơ bị ung thư tuyến giáp, tử cung, vú, cũng như một số bệnh khác. Hội chứng này thường bị gây ra bởi các khiếm khuyết ở gen PTEN.
+ Phức hợp Carney, loại I. Những người mắc hội chứng này có thể phát triển một số khối u lành tính và các vấn đề về hormone. Họ cũng bị tăng nguy cơ ung thư tuyến giáp thể nhú và thể nang. Hội chứng này là do khiếm khuyết ở gen PRKAR1A.
+ Ung thư biểu mô tuyến giáp không phải thể tủy gia đình (familial nonmedullary thyroid carcinoma). Ung thư tuyến giáp xảy ra thường xuyên hơn ở một số gia đình và thường thấy ở độ tuổi sớm hơn. Ung thư tuyến giáp thể nhú thường di truyền trong gia đình. Các gen trên nhiễm sắc thể 19 và nhiễm sắc thể 1 bị nghi ngờ gây ra các ung thư có tính chất gia đình này.
4) Lịch sử gia đình. Có người thân cấp một (cha mẹ, anh, chị em hoặc con) bị ung thư tuyến giáp, ngay cả khi không có hội chứng di truyền trong gia đình, có thể làm tăng nguy cơ bị ung thư tuyến giáp. Cơ sở di truyền của những bệnh ung thư này không hoàn toàn rõ ràng.
1.2.2. Các yếu tố nguy cơ ung thư tuyến giáp có thể thay đổi
1) Sự bức xạ. Sự phơi nhiễm bức xạ là một yếu tố nguy cơ đã được chứng minh đối với bệnh ung thư tuyến giáp. Các nguồn bức xạ gồm một số phương pháp điều trị y tế và bụi phóng xạ từ tai nạn nhà máy điện hoặc vũ khí hạt nhân. Người đã từng xạ trị vùng đầu hoặc cổ khi còn nhỏ là một yếu tố nguy cơ gây ung thư tuyến giáp. Nguy cơ phụ thuộc vào lượng bức xạ được đưa ra và tuổi của trẻ. Việc xạ trị trong thời thơ ấu đối với một số ung thư như ung thư hạch, khối u Wilms và u nguyên bào thần kinh cũng làm tăng nguy cơ ung thư tuyến giáp. Các xét nghiệm hình ảnh như chụp X-quang và chụp CT cũng khiến trẻ em tiếp xúc với bức xạ, nhưng ở liều lượng thấp hơn nhiều. Tuy nhiên, để an toàn, trẻ em không nên thực hiện các xét nghiệm hình ảnh trừ trường hợp thực sự cần thiết. Một số nghiên cứu đã chỉ ra nguy cơ ung thư tuyến giáp ở trẻ em tăng lên do bụi phóng xạ từ vũ khí hạt nhân hoặc tai nạn nhà máy điện hạt nhân (Chernobyl).
2) Thừa cân hoặc béo phì. Nguy cơ ung thư tuyến giáp dường như tăng khi chỉ số khối cơ thể (BMI) tăng.
3) Hàm lượng Iốt trong chế độ ăn uống. Ung thư tuyến giáp thể nang phổ biến hơn ở những khu vực chế độ ăn của người dân có ít i-ốt. Trái lại, chế độ ăn nhiều i-ốt có thể làm tăng nguy cơ ung thư tuyến giáp thể nhú [1].
2. Các dấu hiệu và triệu chứng của ung thư tuyến giáp
Ung thư tuyến giáp có thể gây ra bất kỳ dấu hiệu hoặc triệu chứng nào sau đây:
- Có một khối u ở cổ, đôi khi phát triển nhanh chóng
- Sưng ở cổ
- Đau vùng trước cổ, có khi đau lan lên đến tai
- Khàn tiếng hoặc có những thay đổi khác về giọng nói không biến mất
- Khó nuốt
- Khó thở
- Ho liên tục nhưng không phải do cảm lạnh
Nếu một người có bất kỳ dấu hiệu hoặc triệu chứng nào trong số này, cần đi khám ngay để có thể tìm ra nguyên nhân và điều trị nếu cần. Tuy nhiên, nhiều triệu chứng trong số này cũng có thể do các tình trạng không phải ung thư hoặc là triệu chứng của các bệnh ung thư khác ở vùng cổ gây ra. Các khối u ở tuyến giáp thường là phổ biến và lành tính [1, 2].
3. Các dấu ấn sinh học huyết thanh trong ung thư tuyến giáp
Các xét nghiệm máu thường không được sử dụng để sàng lọc nhằm phát hiện sớm ung thư tuyến giáp vì chúng không đủ độ nhạy và độ đặc hiệu. Tuy nhiên, các xét nghiệm máu có thể giúp đánh giá chức năng tuyến giáp và giúp theo dõi hoạt động của tuyến giáp trong quá trình điều trị ung thư.
1) Hormone kích thích tuyến giáp (TSH). Xét nghiệm nồng độ TSH huyết thanh có thể được sử dụng để kiểm tra hoạt động tổng thể của tuyến giáp.
Nồng độ TSH bình thường là từ 0,45 đến 4,5 mU/L, có nghiên cứu là 0,45 đến 4,12 mU/L. Trong ung thư tuyến giáp, nồng độ TSH huyết thanh thường bình thường.
2) Các hormone tuyến giáp T3 và T4. T3 và T4 là những hormone chính được tạo ra bởi tuyến giáp, cũng có thể được đo để biết chức năng của tuyến giáp.
Nồng độ bình thường của T3 huyết thanh là 80-220 ng/dL và của T4 huyết thanh là 5,0 to 12,0 μg/dL. Trong ung thư tuyến giáp, nồng độ T3 và T4 huyết thanh thường bình thường.
3) Thyroglobulin. Globulin tuyến giáp (thyroglobulin: Tg) là một loại protein được tổng hợp bởi tuyến giáp. Việc đo mức độ thyroglobulin trong máu không được sử dụng để chẩn đoán ung thư tuyến giáp, nhưng có thể hữu ích để theo dõi chức năng tuyến giáp sau điều trị.
Nồng độ bình thường của Tg huyết thanh là 1,40 - 29,2 ng/mL (μg/L) đối với nam và 1,50 - 38,5 ng/mL đối với nữ.
Cách phổ biến nhất để điều trị ung thư tuyến giáp là phẫu thuật cắt bỏ phần lớn tuyến giáp và sau đó sử dụng i-ốt phóng xạ để tiêu diệt các tế bào tuyến giáp còn sót lại. Những phương pháp điều trị này sẽ dẫn đến mức thyroglobulin trong máu rất thấp trong vòng vài tuần. Mức độ Tg không giảm có nghĩa là vẫn còn tế bào ung thư tuyến giáp trong cơ thể. Nếu mức độ Tg tăng trở lại, đó là dấu hiệu cho thấy ung thư có thể tái phát.
4) Calcitonin. Calcitonin là một loại hormone giúp kiểm soát cách cơ thể sử dụng calci. Calcitonin được tạo ra bởi các tế bào C trong tuyến giáp, các tế bào có thể phát triển thành ung thư biểu mô tuyến giáp thể tuỷ (MTC). Nếu nghi ngờ MTC hoặc nếu bạn có tiền sử gia đình mắc bệnh, xét nghiệm máu về nồng độ calcitonin có thể giúp tìm kiếm MTC.
Nồng độ bình thường của calcitonin huyết thanh là ≤19 pg/mL đối với nam và ≤14 pg/mL đối với nữ. Xét nghiệm này có thể được sử dụng để đánh giá khả năng tái phát MTC sau khi điều trị. Vì calcitonin có thể ảnh hưởng đến nồng độ calci máu nên nồng độ calci máu cũng có thể được kiểm tra.
5) Kháng nguyên ung thư bào thai (carcinoembryonic antigen: CEA).
Nồng độ bình thường của kháng nguyên ung thư bào thai (carcinoembryonic antigen: CEA) huyết thanh là 0 - 2,5 ng/mL, nồng độ CEA huyết thanh của những người hút thuốc lá là 0 - 5 ng/mL. Những người bị ung thư biểu mô tuyến giáp thể tuỷ (MTC) thường có nồng độ CEA cao. Xét nghiệm CEA có thể giúp theo dõi ung thư này [1].
Về giá trị của calcitonin và CEA trong chẩn đoán ung thư tuyến giáp thể tủy, giai đoạn càng tăng, độ nhạy chẩn đoán của calcitonin và CEA càng tăng, độ nhạy chẩn đoán của calcitonin cao hơn CEA ở tất cả các giai đoạn. Tuy nhiên, sự kết hợp thêm CEA không làm tăng độ nhạy chẩn đoán của calcitonin (Bảng 1).
Bảng 1. Giá trị của calcitonin và CEA trong chẩn đoán ung thư tuyến giáp thể tủy theo giai đoạn (Kim J, 2021 [6]).
|
Giai đoạn
|
n
|
Số bệnh nhân (+) tính
|
Độ nhạy (%)
|
Giá trị P
|
Tăng độ nhạy khi + CEA
|
|
Calcitonin
|
CEA
|
Calcitonin
|
CEA
|
Calcitonin
|
CEA
|
|
I
|
35
|
31
|
7
|
88,6
|
20,0
|
0,035
|
<0,001
|
0%
|
|
II/III
|
26
|
25
|
15
|
96,2
|
57,7
|
0%
|
|
IV
|
33
|
33
|
29
|
100
|
87,9
|
0%
|
|
Tổng n
|
94
|
89
|
51
|
94,7
|
54,3
|
0%
|
Giá trị dự đoán tái phát của calcitonin và CEA trong ung thư tuyến giáp thể tủy. Giai đoạn càng tăng, độ nhạy dự đoán tái phát của calcitonin và CEA càng tăng, độ nhạy dự đoán tái phát của calcitonin cao hơn CEA ở cả giai đoạn tái phát gần và xa. Tuy nhiên, sự kết hợp thêm CEA không làm tăng độ nhạy dự đoán tái phát của calcitonin (Bảng 1).
Bảng 2. Giá trị theo dõi tái phát của calcitonin và CEA trong ung thư tuyến giáp thể tủy (Kim J, 2021 [6]).
|
Tình trạng tái phát
|
n
|
Số bệnh nhân (+) tính
|
Độ nhạy (%)
|
Tăng độ nhạy khi + CEA
|
|
Calcitonin
|
CEA
|
Calcitonin
|
CEA
|
|
Tái phát tại chỗ
|
25
|
25
|
14
|
100
|
56,0
|
0%
|
|
Tái phát xa
|
20
|
20
|
16
|
100
|
80,0
|
0%
|
6) Procalcitonin (PCT). Trong một nghiên cứu trên 44 bệnh nhân ung thư tuyến giáp thể tủy, trong đó 20 bệnh nhân có bệnh đang hoạt động và 24 bệnh nhân bệnh đã thuyên giảm, Woliński K và cộng sự, 2017 [12], thấy rằng, tất cả các bệnh nhân có bệnh đang hoạt động đều có nồng độ calcitonin huyết thanh vượt quá giới hạn trên bình thường (10 pg/mL), đối với ngưỡng đó, độ nhạy là 100,0% và độ đặc hiệu là 73,9%; ngưỡng phù hợp nhất là 121,0 pg/mL, có độ nhạy 100,0% và độ đặc hiệu là 95,8%. Có sự tương quan rõ rệt giữa calcitonin và procalcitonin (PCT) với P< 0,000001, hệ số tương quan r = 0,93. Tất cả các bệnh nhân có bệnh đang hoạt động đều có PCT vượt quá giới hạn trên của giới hạn bình thường (0,5 ng/mL) với độ nhạy là 100,0% và độ đặc hiệu là 83,3%; ở ngưỡng phù hợp nhất của PCT là 0,95 ng/mL, có độ nhạy 100,0% và độ đặc hiệu là 95,8%. CEA ở ngưỡng tối ưu là 12,66 ng/mL, có độ đặc hiệu là 100,0% và độ nhạy 57,9%. Chromogranin A (CgA) ở ngưỡng tối ưu là 75,66 ng/mL, có độ nhạy 75,0% và độ đặc hiệu 83,3%. Như vậy, procalcitonin (PCT) có thể là một dấu ấn sinh học khối u thay thế cho calcitonin. Việc kết hợp của hai hay nhiều các dấu ấn sinh học khối u có thể làm tăng hiệu quả chẩn đoán, tiên lượng và theo dõi hiệu quả điều trị ung thư tuyến giáp thể tủy.
Các xét nghiệm máu khác. Bệnh nhân cũng có thể có các xét nghiệm máu khác. Nếu bệnh nhân được lên lịch phẫu thuật, các xét nghiệm sẽ được thực hiện để kiểm tra số lượng tế bào máu, tìm các rối loạn chảy máu và kiểm tra chức năng gan và thận.
4. Các dấu ấn sinh học sinh thiết lỏng
Các thành phần chính của sinh thiết lỏng gồm các tế bào khối u lưu thông (circulating tumor cells: CTCs), các DNA khối u lưu thông (circulating tumor DNA: ctDNA), các microRNA (miRNAs) và các túi ngoại bào (exosomes) [3, 4, 5].
4.1. Các tế bào khối u lưu thông (CTCs)
Các tế bào khối u lưu thông (CTCs) là các tế bào khối u lưu thông trong mạch máu hoặc bạch huyết được giải phóng từ các khối u nguyên phát. Các CTC có vai trò hàng đầu trong quá trình di căn, đây là bước quan trọng trong sự tiến triển của các khối u ở các cơ quan xa khác và chịu trách nhiệm cho phần lớn tử vong liên quan đến ung thư. Mặc dù lần đầu tiên vào năm 1869, Thomas Ashworth đã quan sát thấy CTC trong máu của một người đàn ông bị ung thư di căn, tuy nhiên, giá trị của CTC trong nghiên cứu ung thư hiện đại mới được khởi xướng vào giữa những năm 1990 bởi các nhà khoa học ở Philadelphia. Một số nghiên cứu về ung thư đã xác nhận rằng CTC có nguồn gốc từ khối u nguyên phát. Hơn nữa, những nỗ lực đáng chú ý trong việc tìm hiểu các đặc tính sinh học của CTC đã khẳng định vai trò quan trọng của chúng trong sự lây lan di căn của ung thư biểu mô. Cho đến nay, một số công nghệ có độ nhạy và khả năng tái tạo đã giúp xác định CTC ở bệnh nhân ung thư di căn đã được phát triển gần đây [3].
4.2. Các DNA khối u lưu thông (ctDNA)
Các DNA khối u lưu thông (ctDNA) trong máu có chiều dài từ 160 đến 200 cặp bazơ (bp) được các tế bào khối u giải phóng vào máu. Chúng là một đại diện di truyền của khối u chứa các khiếm khuyết di truyền chính xác giống với các tế bào khối u ban đầu. Điều thú vị là tất cả các thay đổi phân tử, bao gồm các đột biến điểm, sự sắp xếp lại, sự khuếch đại và các biến thể sao chép gen đều có thể dễ dàng phát hiện được trong ctDNA của huyết tương. Bệnh nhân ung thư thường có lượng ctDNA cao hơn nhiều so với những người khỏe mạnh từ 0,01%. đến hơn 90%. Hàm lượng ctDNA ở bệnh nhân ung thư có sự tương quan với mức độ của khối u, giai đoạn khối u và hiệu quả của các phương pháp điều trị. Sự thay đổi phân tử cfDNA trong huyết tương có thể thể hiện tình trạng của cơ thể một cách kịp thời, do đó, các đột biến soma cơ bản ở các tế bào bạch cầu (WBC) và cfDNA có thể giúp kiểm soát tình trạng sức khỏe. Để nhận ra mô hình và nguồn đột biến cfDNA, một bảng gồm 50 gen liên quan đến ung thư đã được phân tích ở cả hai nhóm WBC và cfDNA. Hầu hết các đột biến ở cfDNA đều bắt nguồn từ gen WBC và NPM1 là các gen đột biến thường gặp nhất ở cả WBC và cfDNA [3].
4.3. Các miRNA
Vai trò của các miRNA trong ung thư tuyến giáp từ sinh thiết lỏng được thể hiện ở Bảng 3.
Bảng 3. Vai trò của các miRNA trong ung thư tuyến giáp (Mahmoudian-sani MR, 2017 [7])
|
Các miRNA
|
Các gen đích
|
Hoạt động chức năng
|
|
miRNAs-221-222
|
Các gen điều hòa chu kỳ tế bào và chết TB theo chương trình
|
Làm tăng sự phát triển của tế bào, hoạt động của telomere, sự hình thành mạch và quá trình tự thực
|
|
miRNA-375
|
ERBB2
|
Sự biểu hiện quá mức của miRNA này làm tăng sinh tế bào và làm giảm quá trình chết tế bào theo chương trình
|
|
miRNA-155
|
APC
|
Kích hoạt con đường β-catenin, từ đó dẫn đến kích hoạt các con đường xuôi dòng như C-MYC và TCF
|
|
miRNA-146b
|
SMAD4, P27
|
Khi miRNA này bị ức chế, quá trình di chuyển và xâm lấn giảm đáng kể ở các dòng tế bào, đồng thời quá trình di cư và xâm lấn tăng lên bằng sự tăng biểu hiện của nó
|
|
miRNA-34a
|
GAS1
|
Làm tăng hoạt động của con đường PI3K/AKT Bad và có tác dụng chống sự chết tế bào theo chương trình
|
|
miRNA-34a
|
KRAS
|
Ức chế con đường MAPK, ngăn chặn sự tăng sinh tế bào và tăng mức độ biểu hiện P21
|
|
Let-7
|
CYLD
|
Sự giảm biểu hiện của miRNA này dẫn đến tăng sinh tế bào và ức chế quá trình chết theo chương trình ở tế bào ung thư tuyến giáp
|
Ngươi ta thấy rằng các miR-146b-5p, miR-221-3p, và miR-222-3p lưu thông ở bệnh nhân ung thư tuyến giáp thể nhú cao hơn rõ rệt ở trong máu những người khỏe mạnh hoặc bị khối u tuyến giáp lành tính. Nồng độ các miR-146a-5p, miR-146b-5p, miR-221-3p và miR-222-3p giảm rõ rệt ở các bệnh nhân ung thư tuyến giáp thể nhú sau phẫu thuật tuyến giáp [5].
4.4. Các túi ngoại bào
Các túi ngoại bào (exosomes) là các hạt nhỏ có đường kính từ 30 - 100 nm. Các túi ngoại bào có thể tồn tại trong nhiều loại dịch sinh học khác nhau, như huyết tương và nước tiểu. Chúng được giải phóng khỏi tế bào nhân chuẩn khi các thể đa túi hợp nhất với màng sinh chất hoặc được giải phóng ra khỏi màng tế bào. Các túi ngoại bào là một công cụ chẩn đoán ung thư đã được thử nghiệm đối với nhiều ung thư, trong đó có ung thư tuyến giáp. Ưu điểm của các túi ngoại bào là chúng có nhiều trong máu hơn so với CTCs [4, 5].
5. Các thay đổi phân tử và điều tri đích ung thư tuyến giáp
5.1. Các thay đổi phân tử trong ung thư tuyến giáp
Hai con đường tín hiệu MAPK (mitogen - activated protein kinase signaling pathway) và PI3K/AKT (lipid kinase phoshoinositide-3-kinase signaling pathway) là các con đường kích hoạt chính liên quan đến sự hình thành ung thư tuyến giáp. Đột biến BRAF V600E thường gặp ở ung thư biểu mô tuyến giáp thể nhú [10].
Ung thư biểu mô thể nang (follicular thyroid carcinoma) được đặc trưng bởi đột biến RAS và sự dung hợp PAX8-PPARγ. Ung thư tế bào Hürthle (HCC) có các đột biến DNA ty thể, dẫn đến sự tích tụ bất thường của ty thể và kiểu hình tế bào Hürthle, có sự biểu hiện mất nhiễm sắc thể lan rộng và có tần suất đột biến BRAF và RAS thấp.
Ung thư biểu mô tuyến giáp (carcinoma) có sự hình thành khối u phân tử từng bước từ biệt hóa tốt (well-differentiated) đến kém biệt hóa (poorly differentiated) và đến ung thư biểu mô không biệt hóa (anaplastic), trong đó các đột biến BRAF và RAS là nguyên nhân chính.
Đột biến gen khởi động TERT (TERT promoter mutation), đột biến TP53 và đột biến ở con đường PIK3CA có liên quan đến sự xâm lấn của khối u, thường gặp ở ung thư biểu mô tuyến giáp kém biệt hóa và không biệt hóa [10].
Hai con đường tín hiệu MAPK và PI3K/AKT là các con đường kích hoạt chính liên quan đến sự hình thành khối u tuyến giáp. Hai con đường tín hiệu chính có các đột biến gen liên quan đến ung thư tuyến giáp được thể hiện ở Hình 2.
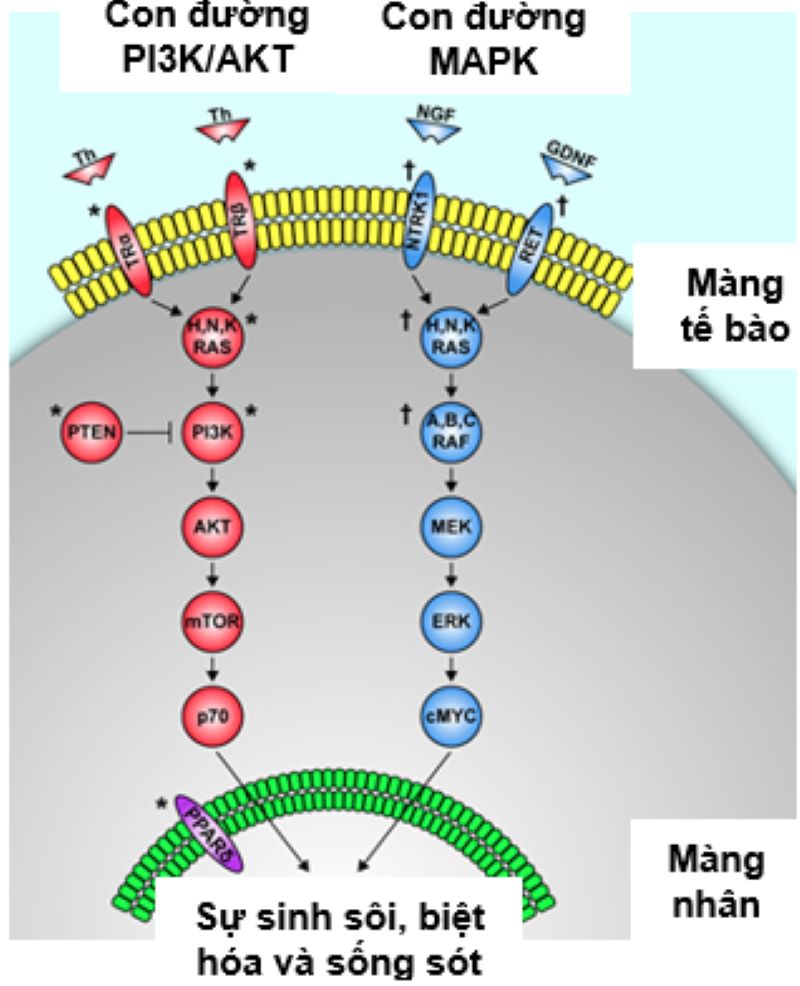
Hình 2. Hai con đường tín hiệu chính có các đột biến gen liên quan đến ung thư tuyến giáp (nguồn: Grogan RH, et al. Cancers 2010)
Các thay đổi phân tử chủ yếu ở các thể ung thư biểu mô tuyến giáp được thể hiện ở Bảng 4.
Bảng 4. Các thay đổi phân tử chủ yếu ở các thể ung thư biểu mô tuyến giáp (Rasheed MRHA và Xu B, 2019 [10])
|
Các loại ung thư tuyến giáp
|
Các thay đổi phân tử hay gặp
|
Các thay đổi phân tử ít gặp
|
|
Ung thư tuyến giáp thể nhú (PTC)
|
BRAF (62%)
Đột biến BRAFV600E là chủ yếu
RAS (13%)
RET-PTC (7%)
Đột biến gen khởi động TERT (9%)
|
E1F1AX
Dung hợp ALK
Dung hợp NTRK1 hoặc NTRK3
|
|
Biến thể dạng nang của ung thư tuyến giáp thể nhú (FVPTC) và u tuyến giáp dạng nang có nhân giống thể nhú (NIFTP)
|
RAS (30-52%)
PAX8-PPARγ (0-38%)
Dung hợp THADA (0-22%)
|
BRAFK601E (3-7%)
Không có đột biến BRAFV600E
|
|
Ung thư tuyến giáp thể nang (FTC)
|
RAS (49%)
PAX8-PPARγ (30-58%)
Đột biến gen khởi động TERT (17%)
|
Các đột biến TSHR
Đột biến BRAFK601E
E1F1AX
|
|
Ung thư biểu mô tế bào Hürthle (HCC)
|
Mất nhiễm sắc thể lan rộng
Thay đổi của bộ gen ty thể
RAS (9-15%)
Đột biến gen khởi động TERT (22-27%)
Đột biến gen TP53 (7-12%)
|
CHCHD10-VPREB3
HEPHL1-PANX1
TMEM233-PRKAB1
|
|
Ung thư tuyến giáp thể kém biệt hóa (PDTC)
|
BRAF 33%
RAS 45%
Đột biến gen khởi động TERT (40%)
Đột biến gen TP53 (10%)
|
|
|
Ung thư tuyến giáp không biệt hóa (ATC)
|
BRAF 29%
RAS 23%
Đột biến gen khởi động TERT (73%)
Đột biến gen TP53 (59%)
|
Các chất ức chế khối u: ATM, RB1, MEN1, NF1 và NF2
Đột biến ảnh hưởng đến con đường PIK3CA-AKT-mTOR, các gen sửa chữa không phù hợp, phức hợp SWI-SNF và con đường histone methyltransferase
|
|
Ung thư tuyến giáp thể tủy (MTC)
|
RET (40-60%)
RAS (up to 20%)
|
MET
Dung hợp ALK
|
Ghi chú: FVPTC (follicular variant of papillary thyroid carcinoma): biến thể dạng nang của ung thư biểu mô tuyến giáp thể nhú, NIFTP (noninvasive follicular thyroid neoplasm with papillary-like nuclear features): u tuyến giáp dạng nang không xâm lấn với các đặc điểm nhân giống thể nhú, PTC (papillary thyroid carcinoma): ung thư biểu mô tuyến giáp thể nhú, FTC (follicular thyroid carcinoma): ung thư biểu mô tuyến giáp thể nang, HCC (Hürthle cell carcinoma): Ung thư biểu mô tế bào Hürthle, PDTC (poorly differentiated thyroid carcinoma): ung thư biểu mô tuyến giáp thể kém biệt hóa, ATC (anaplastic thyroid carcinoma): ung thư biểu mô tuyến giáp thể không biệt hóa, MTC (medullary thyroid carcinoma): ung thư biểu mô tuyến giáp thể tủy.
5.2. Điều trị đích ung thư tuyến giáp
Hầu hết các ung thư tuyến giáp, đặc biệt là ung thư tuyến giáp thể nhú và thể nang đều có khả năng điều trị cao. Hiệu quả điều trị ung thư tuyến giáp phụ thuộc vào loại ung thư tuyến giáp, mức độ tiến triển của bệnh và tình trạng sức khỏe của bệnh nhân. Bên cạnh phẫu thuật (surgery), các phương pháp điều trị ung thư tuyến giáp khác có thể gồm: Liệu pháp i-ốt phóng xạ (radioactive iodine therapy), xạ trị chùm tia bên ngoài (external beam radiation therapy: EBRT), hóa trị liệu (chemotherapy), điều trị hormone (hormone therapy) và điều trị đích (targeted therapy) [1].
Điều trị đích ức chế tyrosine kinase ở con đường MAPK cho thấy kết quả đầy hứa hẹn trong điều trị ung thư biểu mô tuyến giáp tiến triển [8, 10, 11]. Các thuốc điều trị đích trong ung thư biểu mô tuyến giáp tiến triển được thể hiện ở Bảng 5.
Bảng 5. Các thuốc điều trị đích trong ung thư biểu mô tuyến giáp tiến triển (Rasheed MRHA và Xu B, 2019 [10])
|
Các thuốc
|
Các đích
|
Ung thư tuyến giáp được điều trị
|
|
Sorafenib
|
VEGFR, PDGFR, RET/PTC, BRAF, C-KIT
|
Ung thư biểu mô tuyến giáp biệt hóa (DTC) đã điều trị i-ốt phóng xạ (RAI)
Ung thư biểu mô tuyến giáp thể không biệt hóa (ATC)
Ung thư biểu mô tuyến giáp thể tủy (MTC)
|
|
Lenvatinib
|
VEGFR, PDGFR, FGFR, RET/PTC
|
Ung thư biểu mô tuyến giáp biệt hóa (DTC) đã điều trị i-ốt phóng xạ (RAI)
Ung thư biểu mô tuyến giáp thể không biệt hóa (ATC)
Ung thư biểu mô tuyến giáp thể tủy (MTC)
|
|
Cabozantinib
|
VEGFR, RET, MET
|
Ung thư biểu mô tuyến giáp thể tủy (MTC)
|
|
Vandetanib
|
VEGFR, EGFR, RET
|
Ung thư biểu mô tuyến giáp thể tủy (MTC)
|
|
Vemurafenib
|
BRAF
|
Ung thư biểu mô tuyến giáp thể nhú (PTC) có đột biến BRAFV600E đã điều trị i-ốt phóng xạ
|
|
Debrafenib
|
BRAF
|
Ung thư biểu mô tuyến giáp thể nhú (PTC) có đột biến BRAFV600E đã điều trị i-ốt phóng xạ
|
|
Selumtinib
|
MEK1, MEK2
|
Ung thư biểu mô tuyến giáp biệt hóa (DTC) đã điều trị i-ốt phóng xạ (RAI)
|
Ghi chú: DTC (differentiated thyroid carcinoma): ung thư biểu mô tuyến giáp biệt hóa, RAI (radioactive iodine): i-ốt phóng xạ.
Điều trị đích đối với các thể ung thư tuyến giáp cụ thể có thể được thực hiện như sau:
5.2.1. Điều trị đích ung thư tuyến giáp thể nhú hoặc thể nang
Điều may mắn là hầu hết các ung thư tuyến giáp thể nhú hoặc thể nang có thể được điều trị hiệu quả bằng phẫu thuật và liệu pháp i-ốt phóng xạ, do đó ít cần dùng các loại thuốc khác để điều trị. Tuy nhiên, khi những phương pháp điều trị đó không hiệu quả, các loại thuốc điều trị đích có thể là hữu ích.
1) Các thuốc ức chế multikinase. Lenvatinib (Lenvima), sorafenib (Nexavar) và cabozantinib (Cabometyx) là những loại thuốc nhắm đích được gọi là các thuốc ức chế multikinase, vì chúng có thể ngăn chặn một số protein kinase khác nhau. Những loại thuốc này hoạt động bằng 2 cách: Ngăn chặn các khối u hình thành các mạch máu mới mà khối u cần để phát triển và ức chế một số protein được tạo ra bởi các tế bào ung thư vốn giúp chúng phát triển. Lenvatinib và sorafenib thường có thể giúp ngăn chặn sự phát triển ung thư ở những người bị ung thư tuyến giáp biệt hóa (ung thư tuyến giáp thể nhú hoặc nang) mà việc điều trị bằng iốt phóng xạ không còn hiệu quả. Nếu 2 thuốc này không còn hữu ích, cabozantinib có thể là một lựa chọn. Các loại thuốc này đều được dùng bằng đường uống.
2) Các thuốc ức chế RET. Trong ung thư tuyến giáp thể nhú và thể nang, các tế bào có những thay đổi nhất định ở gen RET khiến chúng tạo ra sự bất thường ở RET kinase. Protein bất thường này làm các tế bào phát triển. Selpercatinib (Retevmo) là một loại thuốc ức chế RET. Thuốc này có thể được sử dụng để điều trị ung thư tuyến giáp thể nhú hoặc thể nang tiến triển nếu các tế bào ung thư có sự thay đổi gen RET nhất định và liệu pháp iốt phóng xạ không phải là một lựa chọn tốt. Thuốc này dùng bằng đường uống dạng nang, 2 lần/ ngày.
3) Các thuốc ức chế TRK. Một số kém ung thư tuyến giáp có những thay đổi ở một trong số các gen NTRK. Những thay đổi gen này có thể giúp các tế bào ung thư phát triển. Larotrectinib (Vitrakvi) và entrectinib (Rozlytrek) nhắm đích và vô hiệu hóa các protein TRK bất thường do gen NTRK tạo ra. Mỗi loại thuốc này có thể được sử dụng cho những người bị ung thư tuyến giáp tiến triển có sự thay đổi gen NTRK và đang tiến triển bất chấp các phương pháp điều trị khác. Những thuốc này được dùng dạng viên, 1-2 lần/ ngày.
5.2.2. Điều trị đích ung thư tuyến giáp thể tuỷ
Các bác sĩ đặc biệt quan tâm đến việc tìm ra các loại thuốc nhắm đích để điều trị ung thư tuyến giáp thể tủy (MTC) vì các phương pháp điều trị dựa trên hormone tuyến giáp (bao gồm cả liệu pháp iốt phóng xạ) không hiệu quả đối với các bệnh ung thư này.
1) Các chất ức chế multikinase. Vandetanib (Caprelsa) và cabozantinib (Cometriq) là chất ức chế multikinase (nhắm vào một số protein kinase khác nhau). Chúng tác động đến cả tế bào ung thư và sự sinh các mạch máu mới. Những loại thuốc này có thể được sử dụng để điều trị MTC tiên triển, dưới dạng viên mỗi ngày 1 lần.
2) Các thuốc ức chế RET. Trong ung thư tuyến giáp thể tủy, các tế bào có những thay đổi ở gen RET khiến chúng tạo ra sự bất thường từ protein RET kinase. Protein bất thường này giúp các tế bào phát triển. Selpercatinib (Retevmo) và pralsetinib (Gavreto) là những loại thuốc ức chế RET. Những thuốc này có thể được sử dụng để điều trị MTC tiến triển nếu các tế bào ung thư có một số loại thay đổi gen RET. Selpercatinib được dùng bằng đường uống dưới thể viên nang, 2 lần một ngày. Pralsetinib là viên nang uống mỗi ngày 1 lần.
5.2.3. Điều trị đích ung thư tuyến giáp thể không biệt hóa
Các bác sĩ đã rất quan tâm đến việc tìm ra các loại thuốc nhắm đích để điều trị ung thư tuyến giáp thể không biệt hóa (anaplastic) vì hầu hết các phương pháp điều trị khác đều không hiệu quả đối với các ung thư này.
1) Các thuốc ức chế BRAF và MEK. Một số ung thư tuyến giáp không biệt hóa có những thay đổi ở gen BRAF, khiến chúng tạo ra một số protein để giúp chúng phát triển. Dabrafenib (Tafinlar) và trametinib (Mekinist) là những thuốc nhắm đích vào các protein này. Dabrafenib ức chế protein BRAF, còn trametinib ức chế protein MEK. Những thuốc này có thể được phối hợp để điều trị ung thư tuyến giáp thể không biệt hóa có sự thay đổi ở gen BRAF và không thể loại bỏ hoàn toàn bằng phẫu thuật, dùng dạng viên nén hoặc nang.
2) Các thuốc ức chế RET. Ở một số ung thư tuyến giáp thể không biệt hóa, các tế bào có những thay đổi nhất định ở gen RET khiến chúng tạo ra sự bất thường từ protein RET kinase. Protein bất thường này giúp các tế bào phát triển. Selpercatinib (Retevmo) là một thuốc ức chế RET. Thuốc này có thể được sử dụng để điều trị ung thư tuyến giáp không biệt hóa tiến triển nếu tế bào ung thư có sự thay đổi gen RET. Thuốc này được dùng bằng đường uống dưới thể viên nang, thường là 2 lần/ ngày.
3) Các chất ức chế gen NTRK. Một số ung thư tuyến giáp không biệt hóa có những thay đổi ở gen NTRK. Những thay đổi gen này có thể giúp các tế bào ung thư phát triển. Larotrectinib (Vitrakvi) và entrectinib (Rozlytrek) nhắm đích và vô hiệu hóa các protein TRK bất thường do gen NTRK tạo ra. Mỗi thuốc này có thể được sử dụng cho những người bị ung thư tuyến giáp thể không biệt hóa có sự thay đổi gen NTRK, được dùng dưới dạng viên, 1 hoặc 2 lần/ ngày [1].
Tóm lại, ung thư tuyến giáp là bệnh lý ác tính nội tiết hay gặp nhất, chiếm khoảng 2% tổng số các loại ung thư. Có 5 loại ung thư tuyến giáp chính, gồm Ung thư tuyến giáp thể nhú (80%), thể nang (10%), ung thư tế bào Hurthle (2-3%), thể tủy (2-4%) và thể bất sản (1-2%). Ung thư tuyến giáp có liên quan đến một số bệnh di truyền, nhưng nguyên nhân chính xác của hầu hết các bệnh ung thư tuyến giáp vẫn chưa được biết. Các yếu tố nguy cơ không thể thay đổi gồm: Giới tính và tuổi tác, tình trạng di truyền,… Các yếu tố nguy cơ có thể thay đổi gồm: Bức xạ, thừa cân hoặc béo phì, chế độ ăn nhiều iốt có thể làm tăng nguy cơ ung thư tuyến giáp thể nhú, trong khi chế độ ăn kém iốt có thể làm tăng nguy cơ ung thư tuyến giáp thể nang. Ung thư tuyến giáp có thể gây ra các triệu chứng sau: Có một khối u ở cổ, đôi khi phát triển nhanh chóng, sưng ở cổ, đau ở phía trước cổ, đôi khi đau lên đến tai, khàn giọng hoặc những thay đổi khác về giọng nói không biến mất, khó nuốt, khó thở và ho liên tục không do cảm lạnh. Các xét nghiệm sử dụng để theo dõi ung thư tuyến giáp có thể gồm TSH, T3, T4, Tg và TgAb. Các xét nghiệm đối với ung thư tuyến giáp thể tủy gồm calcitonin, CEA và procalcitonin. Các dấu ấn sinh học dựa trên sinh thiết lỏng có thể gồm: CTCs, cfDNA, miRNAs và EVs. Các con đường tín hiệu chủ yếu trong ung thư tuyến giáp là con đường MAPK và PI3K/AKT. Các thuốc điều trị đích ung thư tuyến giáp thể nhú hoặc thể nang có thể gồm: Các thuốc ức chế Multikinase (lenvatinib, sorafenib và cabozantinib), thuốc ức chế RET (selpercatinib) và các thuốc ức chế TRK (larotrectinib và entrectinib); các thuốc điều trị đích ung thư tuyến giáp thể tủy có thể gồm: Các thuốc ức chế Multikinase (vandetanib và cabozantinib), các thuốc ức chế RET (selpercatinib và pralsetinib); các thuốc điều trị đích ung thư tuyến giáp thể không biệt hóa có thể gồm: các thuốc ức chế BRAF và MEK (dabrafenib và trametinib), thuốc ức chế RET (selpercatinib) và các thuốc ức chế TRK (larotrectinib và entrectinib).
Tài liệu tham khảo
-
ACS. About Thyroid Cancer. Amerian Cancer Society (ACS) 2019.
-
Cancer.Net. Thyroid Cancer Guide. Cancer.Net, 04-2022
-
Jumaah AA, Levy MJ, Reddy N, Bhake R, and Gohil S. Circulating cell-free tumour DNA (ctDNA) utilisation in diagnosis and monitoring of thyroid cancer response to treatment - systematic review. Endocrine Abstracts 2022; 81: 383.
-
Khatami F and Tavangar SM. Liquid Biopsy in Thyroid Cancer: New Insight. Int J Hematol Oncol Stem Cell Res 2018 Jul 1; 12(3): 235-248.
-
Khatami F, Larijani B, Nasiri S, and Tavangar SM. Liquid Biopsy as a Minimally Invasive Source of Thyroid Cancer Genetic and Epigenetic Alterations. Int J Mol Cell Med 2019 Winter; 8(Suppl1): 19-29.
-
Kim J, Park H, Choi MS, et al. Serum Carcinoembryonic Antigen as a Biomarker for Medullary Thyroid Cancer. Int J Thyroidol 2021; 14(2): 143-151.
-
Mahmoudian-sani MR, Mehri-Ghahfarrokhi A, Asadi-Samani M, and Mobinie GR. Serum miRNAs as Biomarkers for the Diagnosis and Prognosis of Thyroid Cancer: A Comprehensive Review of the Literature. Eur Thyroid J 2017 Jul; 6(4): 171-177.
-
Mishra P, Laha D, Grant R, and Nilubol N. Advances in Biomarker-Driven Targeted Therapies in Thyroid Cancer. Cancers (Basel) 2021 Dec; 13(24): 6194.
-
NIH. Surveillance E, and End Results Program. Cancer stat facts: thyroid cancer 9. National Cancer Institute (NIH) 2022.
-
Rasheed MRHA and Xu B. Molecular Alterations in Thyroid Carcinoma. Surg Pathol Clin 2019 Dec; 12(4): 921-930.
-
Tirrò E, Martorana F, Romano C, et al. Molecular Alterations in Thyroid Cancer: From Bench to Clinical Practice. Genes (Basel) 2019 Sep; 10(9): 709.
-
Woliński K, Kaznowski J, Klimowicz A, et al. Diagnostic value of selected biochemical markers in the detection of recurrence of medullary thyroid cancer - comparison of calcitonin, procalcitonin, chromogranin A, and carcinoembryonic antigen. Endokrynol Pol 2017; 68(4): 434-437.


