PGS TS Nguyễn Nghiêm Luật -
Bệnh viện Đa khoa MEDLATEC
Tóm tắt
1) Các yếu tố nguy cơ của ung thư nội mạc tử cung có thể liên quan đến sự tiếp xúc quá mức của nội mạc tử cung với estrogen, bao gồm liệu pháp estrogen không bị đối kháng, có kinh sớm, mãn kinh muộn, điều trị tamoxifen, chưa sinh đẻ, vô sinh hoặc không rụng trứng và hội chứng buồng trứng đa nang. Các yếu tố nguy cơ khác là tuổi tăng, béo phì, tăng huyết áp, đái tháo đường và ung thư đại trực tràng không đa polyp di truyền.
2) Các dấu hiệu và triệu chứng của ung thư nội mạc tử cung có thể bao gồm: Chảy máu âm đạo sau khi mãn kinh, chảy máu giữa các kỳ kinh, đau vùng chậu, có một khối u và sút cân.
3) Các dấu ấn sinh học khối u huyết thanh đối với ung thư nội mạc tử cung có thể bao gồm: CA125 là dấu ấn chính trong chẩn đoán, theo dõi và tiên lượng ung thư nội mạc tử cung; HE4 có tiềm năng tốt hơn để sử dụng trong chẩn đoán ung thư nội mạc tử cung so với CA125; sự kết hợp của CA125 và HE4 có thể được áp dụng để theo dõi sự tái phát, sự xâm lấn vào cơ tử cung, di căn hạch bạch huyết và tiên lượng ở bệnh nhân ung thư nội mạc tử cung.
4) Sinh thiết chất lỏng (LB) ở bệnh nhân ung thư nội mạc tử cung bao gồm một số dịch sinh học như máu, nước tiểu, dịch/nước rửa phúc mạc và các dấu ấn sinh học như các tế bào khối u lưu thông (CTCs), các DNA khối u lưu thông (ctDNAs), RNA không mã hóa dài (lncRNA), microRNA (miNA), các vi túi lưu thông (cMVs) hoặc các túi ngoại bào, các tiểu cầu nuôi khối u (TEPs), mRNA (mRNA) và protein có thể đóng các vai trò khác nhau trong chẩn đoán, tiên lượng và quản lý bệnh nhân cũng như giúp nâng cao kiến thức về sự tiến triển của ung thư này.
5) Các con đường tín hiệu phân tử chính của ung thư nội mạc tử cung bao gồm con đường tín hiệu RTK, con đường tín hiệu Wnt, con đường tín hiệu Notch, con đường tín hiệu p53 và p16. Các điều trị đích ung thư nội mạc tử cung bao gồm: (1) Các chất ức chế thụ thể yếu tố tăng trưởng biểu bì (EGFR) kinase; (2) các chất ức chế sự hình thành mạch máu; (3) các chất ức chế mTOR, và các thử nghiệm lâm sàng giai đoạn 2 đang diễn ra bao gồm (4) các chất ức chế điểm kiểm soát miễn dịch và (5) các chất ức chế poly (ADP-ribose) polymerase (PARP).
*
Endometrian Cancer: Serum tumor biomarkers, liquid biopsy-based biomarkers, molecular alterations and targeted therapy
Luat Nghiem Nguyen
MEDLATEC General Hospital
Abstract
1) Risk factors of endometrial cancer can are related to excessive unopposed exposure of the endometrium to estrogen, including unopposed estrogen therapy, early menarche, late menopause, tamoxifen therapy, nulliparity, infertility or failure to ovulate, and polycystic ovary syndrome. Additional risk factors are increasing age, obesity, hypertension, diabetes mellitus, and hereditary nonpolyposis colorectal cancer.
2) Signs and symptoms of endometrial cancer may include: Vaginal bleeding after menopause, bleeding between periods, pelvic pain, a mass, and weight loss.
3) Serum tumor biomarkers for endometrial cancer can include: CA125 is the major marker in the diagnosis, monitoring and prognosis of endometrial cancer; HE4 has a good potential for use in diagnosis of endometrial cancer compared to CA125; the combination of CA125 and HE4 could be applied to monitor recurrence, deep myometrial invasion, lymph node metastasis and prognosis in endometrial cancer patients.
4) Liquid biopsy (LB) in patients with endometrial cancer includes several biofluids such as blood, urine, peritoneal fluid/lavage, and biomarkers such as circulating tumor cells (CTCs), circulating tumor DNA (ctDNAs), long noncoding RNA (lncRNA), microRNA (miNA), circulating microvesicles (cMVs) or exosomes, tumor educated platelets (TEPs), mRNA (mRNA), and proteins that can play different roles in diagnosis, prognosis, and patient management as well as in the improvement of the knowledge of the cancer evolution.
5) The main molecular signaling pathways of endometrial cancer including RTK signaling pathway, Wnt signaling pathway, Notch signaling pathway, as well as p53 and p16 signaling pathway. Targeted therapies for endometrial cancer include: (1) Epidermal growth factor receptor (EGFR) kinase inhibitors; (2) angiogenesis inhibitors; and (3) mTOR inhibitors and ongoing phase 2 clinical trials, including (4) immune checkpoint inhibitors and (5) poly (ADP-ribose) polymerase (PARP) inhibitors.
*
Tử cung (uterine) là cơ quan vùng chậu rỗng, hình quả lê, nơi diễn ra sự phát triển của thai nhi. Ung thư nội mạc tử cung (endometrial cancer), còn được gọi là ung thư tử cung (uterine cancer), bắt nguồn từ lớp tế bào hình thành lớp nội mạc tử cung (endometrium) của tử cung. Một loại ung thư khác cũng có thể được hình thành trong tử cung nhưng ít phổ biến hơn nhiều là sarcoma tử cung (uterine sarcoma) (Hình 1).
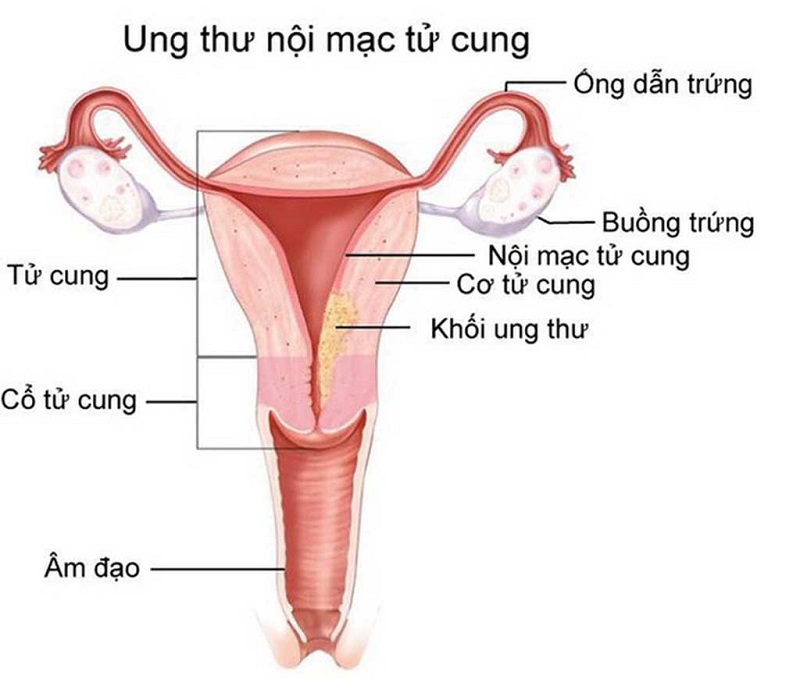
Hình 1. Ung thư nội mạc tử cung (Nguồn: Endometrial cancer, Mayo Clinic, May 20, 2021).
Về tỷ lệ mắc, ung thư nội mạc tử cung đứng thứ 6 về tỷ lệ mắc ở phụ nữ trên toàn thế giới, theo dữ liệu của GLOBOCAN 2020, với 417.367 ca mới vào năm 2020 và nguy cơ tích lũy (cumulative risk) là 1,6% [13]. Khoảng 70% ung thư nội mạc tử cung có thể được chẩn đoán ở giai đoạn sớm. Tiên lượng của ung thư nội mạc tử cung sẽ thuận lợi nếu được chẩn đoán ở giai đoạn sớm và sẽ kém nếu được chẩn đoán ở giai đoạn muộn. Vì vậy, việc phát hiện, chẩn đoán và điều trị sớm có thể giúp nâng cao tỷ lệ sống của bệnh nhân ung thư nội mạc tử cung [6].
Về phân loại, trước năm 2013, ung thư nội mạc tử cung được chia thành hai loại, loại phụ thuộc vào estrogen (loại I) và loại không phụ thuộc vào estrogen (loại II), theo phân loại cổ điển của Bokhman. Việc đánh giá mô bệnh học bao gồm loại và mức độ của khối u, cùng với các yếu tố lâm sàng được coi là những yếu tố tiên lượng rất quan trọng ảnh hưởng đến quyết định điều trị. Tuy nhiên, các khối u giống nhau về mặt mô học có thể có các hậu quả khác nhau. Các phát hiện phân tử gần đây và các thông số mô bệnh học mới đã cho khái niệm mới về phân tầng nguy cơ, về quản lý ung thư và đã phân ung thư nội mạc tử cung thành 4 phân nhóm phân tử (molecular subgroups), gồm: 1) phân nhóm cực kỳ đột biến (POLE ultramutated: POLE mut), phân nhóm đột biến p53 (p53 mutant: p53abn), phân nhóm thiếu sự sửa chữa không phù hợp (mismatch repair deficient: MMRd) và phân nhóm cấu hình phân tử không đặc hiệu (non-specific molecular profile: NSMP) [3, 4, 15].
Về tiên lượng, ung thư nội mạc tử cung thường được phát hiện ở giai đoạn sớm vì thường gây chảy máu âm đạo bất thường. Nếu được phát hiện sớm, với phẫu thuật cắt bỏ tử cung, ung thư nội mạc tử cung có thể có tiên lượng tốt hơn nhiều. Ở những bệnh nhân có khối u khu trú trong tử cung, tỷ lệ sống sót sau 5 năm là ≥ 95%, nhưng tỷ lệ này giảm đột ngột khi khối u đã di căn khỏi tử cung, với tỷ lệ tỷ lệ sống sót sau 5 năm là 69% ở những bệnh nhân có di căn quanh vùng và là 17% ở những bệnh nhân có di căn xa [15].
Trong bài viết này, các yếu tố nguy cơ, các dấu hiệu và triệu chứng, các dấu ấn sinh học khối u huyết thanh, các dấu ấn sinh học dựa trên sinh thiết lỏng, các thay đổi về phân tử và điều trị đích trong ung thư nội mạc tử cung sẽ được trình bày.
1. Các nguyên nhân và yếu tố nguy cơ
1.1. Các nguyên nhân
Nguyên nhân của ung thư nội mạc tử cung hiện còn chưa được rõ. Người ta cho rằng những thay đổi (đột biến) ở DNA của các tế bào trong nội mạc tử cung có thể biến các tế bào bình thường, khỏe mạnh thành các tế bào bất thường. Các tế bào khỏe mạnh phát triển và nhân lên theo một tốc độ nhất định, cuối cùng sẽ chết vào một thời điểm nhất định. Các tế bào bất thường phát triển và nhân lên ngoài tầm kiểm soát và không chết vào một thời điểm nhất định. Các tế bào bất thường tích tụ tạo thành một khối u. Tế bào ung thư xâm lấn các mô lân cận và có thể tách ra khỏi khối u ban đầu để di căn sang nơi khác trong cơ thể.
1.2. Các yếu tố nguy cơ
Các yếu tố nguy cơ ung thư nội mạc tử cung có thể bao gồm:
1) Các yếu tố nguy cơ ung thư nội mạc tử cung liên quan đến sự tiếp xúc quá mức của nội mạc tử cung với estrogen, bao gồm liệu pháp estrogen không bị đối kháng (unopposed estrogen therapy), nghĩa là việc điều trị thay thế estrogen không có các progestin, có thể làm tăng nguy cơ ung thư nội mạc tử cung, có kinh đầu tiên sớm (early menarche), mãn kinh muộn (late menopause), liệu pháp tamoxifen, chưa sinh đẻ (nulliparity), vô sinh (infertility) hoặc không rụng trứng (failure to ovulate) và hội chứng buồng trứng đa nang (polycystic ovary syndrome).
2) Các yếu tố nguy cơ ung thư nội mạc tử cung khác có thể gồm tuổi tăng, béo phì, tăng huyết áp, đái tháo đường và ung thư đại trực tràng không đa polyp di truyền (hereditary nonpolyposis colorectal cancer) (theo Braun MM, 2016 Mar 15).
2. Các dấu hiệu và triệu chứng
Khoảng 75% phụ nữ bị ung thư nội mạc tử cung là sau mãn kinh, triệu chứng phổ biến nhất là chảy máu sau mãn kinh. Đối với 25% ung thư nội mạc tử cung còn lại xảy ra ở bệnh nhân tiền mãn kinh (perimenopausal hoặc premenopausal), các triệu chứng gợi ý về ung thư nội mạc tử cung có thể ít hơn (theo Creasman WT, 2022 Apr 04).
Các dấu hiệu và triệu chứng của ung thư nội mạc tử cung có thể bao gồm:
1) Chảy máu âm đạo bất thường, có vết máu hoặc bài tiết dịch khác. Khoảng 90% phụ nữ bị ung thư nội mạc tử cung bị chảy máu âm đạo bất thường. Điều này có thể là sự thay đổi trong kỳ kinh của họ, chảy máu giữa các kỳ kinh ở thời kỳ tiền mãn kinh hoặc chảy máu sau khi mãn kinh. Các vấn đề không phải ung thư cũng có thể gây chảy máu bất thường. Nếu một phụ nữ đã trải qua thời kỳ mãn kinh, điều đặc biệt quan trọng là phải báo cáo bất kỳ hiện tượng chảy máu âm đạo, ra máu hoặc tiết dịch bất thường nào cho bác sĩ. Tiết dịch âm đạo không lẫn máu cũng có thể là dấu hiệu của ung thư nội mạc tử cung. Khi có bất kỳ một dịch tiết bất thường nào nên được bác sĩ kiểm tra.
2) Đau vùng chậu, có khối u vùng chậu và sụt cân. Đau ở vùng xương chậu, cảm thấy có khối u và sụt cân không rõ nguyên nhân cũng có thể là các triệu chứng của ung thư nội mạc tử cung. Các triệu chứng này phổ biến hơn trong giai đoạn sau của bệnh. Tuy nhiên, bất kỳ sự chậm trễ nào trong việc tìm kiếm trợ giúp y tế có thể khiến bệnh tiến triển thêm. Điều này làm giảm tỷ lệ điều trị thành công. Vì vậy, một phụ nữ khi có bất kỳ triệu chứng nào trong số các triệu trứng trên đều cần đi khám bệnh để bác sĩ kiểm tra (theo ACS 2022).
3. Các dấu ấn sinh học khối u huyết thanh
Các dấu ấn khối u sinh học huyết thanh thường được sử dụng trong chẩn đoán, theo dõi hiệu quả điều trị và tiên lượng ung thư nội mạc tử cung là CA125 và HE4. Giới han tham chiếu ở người khỏe mạnh bình thường của nồng độ CA-125 và HE4 huyết thanh tương ứng là <35 U/mL và <140 pmol/L.
Về sàng lọc, CA125 không đủ độ nhạy và độ đặc hiệu để sàng lọc nhằm phát hiện sớm ung thư nội mạc tử cung vì nồng độ trong huyết thanh chỉ tăng ở 10-20% phụ nữ bị ung thư nội mạc tử cung giai đoạn sớm và chỉ ở 25% bệnh nhân bị tái phát không triệu chứng. Ngoài ra, cũng còn vì nồng độ CA125 cũng có thể tăng trong một số bệnh lành tính.
Về chẩn đoán, trong một nghiên cứu trên 150 bệnh nhân ung thư nội mạc tử cung, 100 bệnh nhân bị các bệnh tử cung lành tính và nhóm đối chứng gồm 100 phụ nữ khỏe mạnh, Dong C và cộng sự, 2017 [6], sử dụng các điểm cắt tối ưu (optimal diagnosis cut-off point) của CA125 là 31,32 U/mL và của HE4 là 92,21 pmol/L, thấy rằng có sự khác biệt có ý nghĩa về số ca âm tính và dương tính của HE4 và CA125 giữa nhóm ung thư nội mạc tử cung, nhóm bệnh tử cung lành tính và nhóm đối chứng khỏe mạnh (P<0,05). Tuy nhiên, không có sự khác biệt có ý nghĩa thống kê giữa nhóm bệnh tử cung lành tính và nhóm đối chứng khỏe mạnh (P>0,05) (Bảng 1).
Bảng 1. So sánh các tình trạng âm tính và dương tính của CA125 và HE4 với các điểm cắt tối ưu [6].
|
Nhóm
|
n
|
CA125
|
HE4
|
|
(-) tính
|
(+) tính
|
(-) tính
|
(+) tính
|
|
Ung thư nội mạc tử cung
|
150
|
73
|
77
|
65
|
85
|
|
Các bệnh tử cung lành tính
|
100
|
94*
|
6*
|
93*
|
7*
|
|
Nhóm đối chứng
|
100
|
92*#
|
8*#
|
97*#
|
3*#
|
Ghi chú: *P<0,05 nhóm đối chứng so với nhóm ung thư nội mạc tử cung; #P>0,05 nhóm đối chứng so với nhóm các bệnh tử cung lành tính.
Dong C và cộng sự, 2017 [6] còn thấy rằng, độ nhạy, độ đặc hiệu, giá trị dự đoán âm tính, giá trị dự đoán dương tính ung thư nội mạc tử cung của HE4 đều cao hơn so với CA125. Các giá trị này của sự kết hợp CA125 và HE4 cũng đều cao hơn các giá trị tương ứng của từng dấu ấn khối u riêng rẽ (Bảng 2).
Bảng 2. So sánh giá trị của CA125, HE4 và sự kết hợp của chúng trong chẩn đoán ung thư nội mạc tử cung [6].
|
Dấu ấn khối u
|
Độ nhạy (%)
|
Độ đặc hiệu (%)
|
NPV (%)
|
PPV (%)
|
|
CA125
|
51,7
|
93,9
|
73,7
|
85,2
|
|
HE4
|
57,2
|
95,8
|
76,5
|
89,6
|
|
CA125+HE4
|
73,2
|
91,2
|
83,4
|
84,8
|
Ghi chú: NPV (negative predictive value): Giá trị dự báo (-) tính; PPV (positive predictive value): Giá trị dự báo (+) tính.
Về dự đoán sự tiến triển của ung thư nội mạc tử cung, nồng độ HE4 huyết thanh cũng đã được chứng minh là có tương quan với mức độ sâu của sự xâm lấn nội mạc tử cung và giai đoạn của ung thư biểu mô nội mạc tử cung [16].
Về tiên lượng ung thư nội mạc tử cung, nồng độ CA 125 >35 U/mL là một yếu tố dự báo độc lập cho tỷ lệ sống thấp. Giá trị trước phẫu thuật của HE4 và CA 125 có thể được sử dụng để đánh giá thời gian sống sót tổng thể (overall survival: OS) và thời gian sống không bệnh (disease-free survival: DFS). Sự kết hợp của hai dấu hiệu này là dấu ấn tốt để dự đoán thời gian sống sót [5, 12].
4. Các dấu ấn sinh học sinh thiết lỏng
Sinh thiết lỏng (liquid biopsy: LB) là một công cụ mới để đánh giá sự tái phát của một số ung thư và ngày nay được sử dụng trong nhiều ung thư để phát hiện ban đầu và xác định đặc điểm phân tử khi không có mô sinh thiết khối u. Sinh thiết lỏng bao gồm một số chất liệu sinh học như máu, nước tiểu, dịch/ nước rửa phúc mạc và các dấu ấn sinh học dựa trên sinh thiết lỏng (liquid biobsy-based biomarkers) hay dấu ấn sinh học sinh thiết lỏng (liquid biobsy biomarkers) như các tế bào khối u lưu thông (circulating tumor cells: CTCs), các DNA khối u lưu thông (circulating tumor DNA: ctDNA), RNA không mã hóa dài (long noncoding RNA: lnRNA), các microRNA (microRNAs), các các vi túi lưu thông (circulating microvesicles: cMVs) hoặc các túi ngoại bào (exosomes), các tiểu cầu nuôi khối u (tumor educated platelets: TEPs), các mRNA và các protein. Các dấu ấn sinh học dựa trên sinh thiết lỏng có thể có các vai trò khác nhau trong chẩn đoán, tiên lượng và quản lý bệnh nhân, cũng như giúp nâng cao kiến thức về sự tiến triển của ung thư nội mạc tử cung [9].
Các kỹ thuật giải trình tự thế hệ tiếp theo (next-generation sequencing: NGS) và sinh thiết lỏng (LB) là những công nghệ mới có thể cho phép xác định tổng thể khối u trong một phân tích duy nhất và đóng một vai trò quan trọng trong điều trị đích (targeted therapy) - một phương pháp điều trị ung thư học chính xác (precision oncology).
Sơ đồ tổng quan về các mẫu sinh học của sinh thiết lỏng, các dấu ấn sinh học và các ứng dụng lâm sàng của chúng trong ung thư nội mạc tử cung được thể hiện ở Hình 2.
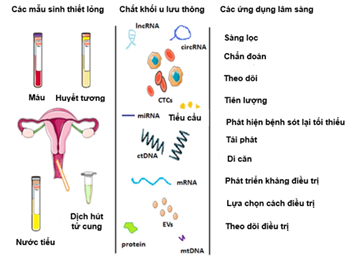
Hình 2. Sơ đồ tổng quan về các mẫu sinh học của sinh thiết lỏng, các dấu ấn sinh học và các ứng dụng lâm sàng của chúng trong ung thư nội mạc tử cung [9]. CTCs (circulating tumor cells): các tế bào khối u lưu thông; ctDNA (circulating tumor DNA): DNA khối u lưu thông; cMVs (circulating microvesicles): các vi túi lưu thông; MRD (minimal residual disease): bệnh sót lại tối thiểu.
Các nghiên cứu lâm sàng gần đây cho thấy một số ứng dụng lâm sàng tiềm năng của các dấu ấn sinh học sinh thiết lỏng đang trở thành hiện thực (Bảng 3).
Bảng 3. Các ứng dụng lâm sàng tiềm năng của các dấu ấn sinh học sinh thiết lỏng [11].
|
Sinh thiết lỏng
|
Các kỹ thuật phát hiện
|
Các dấu ấn sinh học
|
Ứng dụng lâm sàng
|
|
Dịch hút tử cung
|
Bộ protein (proteomics) đích
|
ABRACL và PGAM2; KPYM, MMP9, để xác định bệnh; CTNB1, XPO2 và CAPG để phân biệt giữa ung thư biểu mô nội mạc tử cung (EEC) và ung thư biểu mô nội mạc tử cung dạng huyết thanh (SEC)
|
Chẩn đoán
|
|
Giải trình tự đích
|
PTEN, PIK3CA, CTNNB1, TP53, FGFR2, KRAS, CDKN2A (các gen bị đột biến phổ biến nhất trong ung thư nội mạc tử cung (EC)
|
Chẩn đoán
|
|
Các tế bào khối u lưu thông (CTCs)
|
Miễn dịch dựa trên EpCAM (CellSearch®) và IF
|
CK-8, CK-18, CK-19, ETV5, NOTCH1, SNAI1, TGFB1, ZEB1 và ZEB2
|
Tiên lượng
|
|
Làm giàu dựa trên mật độ và RTqPCR
|
CCNE2, DKFZp762E1312, EMP2, MAL2, PPIC và SLC6A8
|
Tiên lượng
|
|
RTqPCR và đo tế bào dòng chảy
|
TTF-1 và biểu hiện mRNA của: Survivin, β-catenin, miR-15a, và PTEN
|
Tiên lượng
|
|
Các CTC được làm giàu dựa trên kích thước (Metacell®) và phát hiện miễn dịch
|
Các CTC được xác định dựa trên: 1) kích thước tế bào ≥15 μm; 2) kích thước nhân ≥10 μm); 3) sự bất thường của đường viền hạt nhân; 4) tế bào chất nhìn thấy được; 5) nucleoli nổi bật; 6) tỷ lệ nhân-bào tương; 7) sự hiện diện của cụm; 8) hiện diện nguyên phân.
|
Tiên lượng
|
|
Các tiền tế bào nội mô (EPC)
|
Tế bào dòng chảy
|
VEGFR2/KDR và CD34
|
Chẩn đoán
|
|
DNA không tế bào (cfDNA)
|
PCR-RFLP
RTqPCR
Alu-RTqPCR
NGS
|
KRAS
Các chuỗi Alu
Hàm lượng cfDNA và chỉ số toàn vẹn
Các biến thể số sao chép (CNVs)
|
Tiên lượng
Tiên lượng
Tiên lượng
Chẩn đoán
|
|
DNA khối u lưu thông (ctDNA)
|
Phản ứng PCR kỹ thuật số dạng giọt
|
Sự dung hợp và các đột biến đặc hiệu trong các ctDNA
|
Đáp ứng điều trị
|
|
miRNA lưu thông
|
RTqPCR
|
miR-99a/miR-199b, miR-9/miR-1228 và miR-9/miR-92a, miR-222, miR-223, miR-186, miR-204 và miR-21
|
Chẩn đoán/ Tiên lượng
|
5. Những thay đổi phân tử và điều trị đích ung thư nội mạc tử cung
Một số cơ chế có thể dẫn đến sự sinh ung thư và di căn, bao gồm ức chế quá trình chết theo chương trình (apoptosis), gây tăng sinh tế bào, tăng cường phiên mã TERT và sự can thiệp vào quá trình sửa chữa DNA. Các con đường tín hiệu phân tử chính của ung thư nội mạc tử cung bao gồm con đường tín hiệu RTK, con đường tín hiệu Wnt, con đường tín hiệu Notch, cũng như con đường tín hiệu p53 và p16. Các con đường phân tử của các gen ARID1A, PTEN, KRAS, CTNNB1 và MMR chỉ ảnh hưởng đến khối u nội mạc tử cung, trong khi các khối u tử cung thanh dịch thường chứa các biến đổi ở các gen TP53, HER2, p16, CCNE1 và FBXW7.
5.1. Những thay đổi phân tử trong ung thư nội mạc tử cung
Hầu hết các loại ung thư nội mạc tử cung là ung thư biểu mô (carcinoma), thường là ung thư biểu mô tuyến (adenocarcinoma). Chúng phát triển từ một lớp tế bào biểu mô lót nội mạc tử cung. Có một số loại phụ của ung thư biểu mô nội mạc tử cung, được phân loại thành hai loại, dựa trên các đặc điểm lâm sàng và cơ chế bệnh sinh:
Ung thư nội mạc tử cung loại I: Ung thư nội mạc tử cung loại I thường phát triển trước thời kỳ mãn kinh. Những biểu hiện này phổ biến hơn ở những người da trắng đã bị tăng sản nội mạc tử cung. Những bệnh ung thư này thường xâm lấn tối thiểu và có tỷ lệ sống sót khi điều trị. Khoảng 70-90% ung thư nội mạc tử cung thuộc loại 1.
Ung thư nội mạc tử cung loại II: Ung thư nội mạc tử cung loại II thường xảy ra ở phụ nữ lớn tuổi, sau mãn kinh, phổ biến hơn ở phụ nữ da đen, và không phụ thuộc vào việc tiếp xúc với estrogen hoặc tiền sử tăng sản nội mạc tử cung.
Ung thư biểu mô nội mạc tử cung được chia thành các loại phụ mô học khác nhau, gồm:
1) Ung thư biểu mô tuyến nội mạc tử cung (endometrioid adenocarcinomas: EEC).
2) Ung thư biểu mô thanh dịch (serous carcinomas: SC).
3) Ung thư biểu mô tế bào sáng (clear cell carcinomas: CCC).
4) Sarcoma biểu mô tử cung (uterine carcinosarcoma: UCS).
5) Các ung thư biểu mô khác như: Ung thư biểu mô nhầy (mucinous), ung thư biểu mô nội tiết thần kinh (neuroendocrine), ung thư biểu mô không biệt hóa (undifferentiated), và ung thư biểu mô mất biệt hóa (dedifferentiated carcinoma).
Năm 2013, Tổ chức Bản đồ Bộ gen Ung thư (The Cancer Genome Atlas: TCGA) cho rằng ung thư biểu mô nội mạc tử cung một bệnh không đồng nhất nên đã phân loại phân tử ung thư này thành bốn phân nhóm:
1) Các ung thư nội mạc tử cung chứa cực kỳ nhiều đột biến ở gen POLE (ultramuted-POLE mut ECs), chứa cực kỳ nhiều các đột biến gây bệnh ở gen POLE;
2) Các ung thư nội mạc tử cung thiếu hụt sự sửa chữa ghép đôi sai lệch do siêu đột biến gen MMR (hypermuted-mismatch repair deficient: MMRd), thể hiện sự không ổn định vi mô (microsatellite instability: MSI);
3) Các ung thư nội mạc tử cung có số bản sao thấp (copy-number low), là một nhóm không có cấu hình phân tử đặc hiệu (a group with no specific molecular profile: NSMP); và 4) các ung thư nội mạc tử cung gen TP35 giống thanh dịch có số bản sao cao (copy-number high-serous-like TP35 EC), có các đột biến ở gen TP53 (p53abn).
Những thay đổi phân tử (molecular alterations) trong ung thư nội mạc tử cung bao gồm những đột biến gen và những thay đổi protein có thể xảy ra trên các con đường tín hiệu phân tử (molecular signaling pathways) như các con đường tín hiệu phân tử RTK, Wnt, Notch, p53 và p16. Tần suất của những thay đổi phân tử của các đích phổ biến nhất trong ung thư nội mạc tử cung theo các kiểu phụ mô học (histological subtypes) được thể hiện ở Bảng 4.
Bảng 4. Tần suất của những thay đổi phân tử của các đích phổ biến nhất trong ung thư nội mạc tử cung theo loại phụ mô học [14].
|
Những thay đổi phân tử
|
Ung thư biểu mô tuyến nội mạc tử cung (EEC)
|
Ung thư biểu mô tuyến thanh dịch (SC)
|
Ung thư biểu mô tế bào sáng (CCC)
|
Carcinosarcoma tử cung (UCS)
|
|
Đột biến gen PTEN
|
64-80% G1-3, 52-82% G1/G2, 62-90% G3
|
2-3%
|
0-21%
|
11-33%
|
|
Đột biến gen PI3KCA
|
22-59% G1-G3, 38-54% G1/G2, 45-59% G3
|
15-35%
|
24-36%
|
22-40%
|
|
Đột biến gen PIK3R1
|
9-43% G1-G3, 19-38% G1/G2, 31-41% G3
|
5-8%
|
7-18%
|
6-20%
|
|
Đột biến gen KRAS
|
19-43% G1-G3, 17-23% G1/G2, 7-33% G3
|
2-6%
|
2-14%
|
10-17%
|
|
Đột biến gen FGFR2
|
10-18% G1-G3, 11-13% G1/G2, 14-16% G3
|
8%
|
0%
|
0-2%
|
|
Đột biến gen CTTNB1
|
19-37% G1-G3, 24-28% G1/G2, 19-40% G3
|
0-3%
|
0%
|
0-5%
|
|
MMR-d
|
34-35% G1-G3, 34% G1/G2, 44% G3
|
0-3%
|
11-14%
|
3-6%
|
|
Đột biến gen ARID1A
|
39-55% G1-G3, 39-47% G1/G2, 39-60% G3
|
7-11%
|
14-21%
|
10-24%
|
|
Đột biến gen P53
|
5-14% G1-G3, 6-10% G1/G2, 21-35% G3
|
59-93%
|
28-46%
|
44-91%
|
|
Khuếch đại ERBB2
|
1% G1-G3, 3% G1/G2, 4% G3
|
26-44%
|
11%
|
9%
|
|
Đột biến gen POLE
|
13-15% G1-G3,11% G1/G2, 20% G3
|
0-2%
|
2-7%
|
3-4%
|
Ghi chú: Ghi chú: PIK3CA (phosphatidylinositol 3-kinase catalytic subunit): đơn vị xúc tác phosphatidylinositol 3-kinase; FGFR2 (fibroblast growth factor receptor 2): thụ thể yếu tố tăng trưởng nguyên bào sợi 2; PTEN (phosphatase and tensin homolog): chất tương đồng phosphatase và tensin; Bax (BCL2-associated X protein): protein X liên quan đến BCL2; MMRd (MMR deficiency): suy giảm protein MMR do đột biến gen ghép cặp không phù hợp (mismatch repair (MMR) genes); POLE (p261) mã hóa cho DNA polymerase ε, là một protein enzym gồm 4 tiểu đơn vị không đồng dạng (heterotetramer) là p261, p59, p17 và p12.
Mười gen đột biến hàng đầu trong ung thư nội mạc tử cung gồm: PTEN (57%), PIK3CA (48%), TTN (44%), ARID1A (43%), TP53 (36%), MUC16 (30%), PIK3R1 (30%) ), KMT2D (27%), CTCF (24%) và CSMD3 (24%). Ngoài ra, 15% bệnh nhân ung thư nội mạc tử cung cũng có đột biến soma POLE, mã hóa cho DNA polymerase ε, trong đó hơn 90% đột biến POLE là các đột biến nhầm nghĩa (missense mutations).
Đột biến ở các gen PIK3CA, ARID1A, TP53, PIK3R1 và MUC16 có liên quan đến tiên lượng, trong số đó, đột biến ở các gen PIK3CA, ARID1A và MUC16 tương quan với tiên lượng thuận lợi, trong khi đột biến ở các gen TP53 và PIK3R1 tương quan với tiên lượng kém.
Tuy nhiên, không phải những thay đổi phân tử nào trong ung thư cũng đều là mục tiêu cho các điều trị đích. Các phân tử đích đang được thử nghiệm lâm sàng đối các điều trị đích tiềm năng (potential targeted therapies) trong ung thư nội mạc tử cung được biểu hiện ở Bảng 5.
Bảng 5. Các phân tử đích đang được thử nghiệm lâm sàng trong ung thư nội mạc tử cung [10].
|
Các điều trị đích
|
Các phân tử đích
|
|
Ức chế điểm kiếm soát miễn dịch (ICI)
|
PD-1, PD-L1, CTLA4, GITR, OX40, arginase, IDO1, TLR7
|
|
Chống tăng sinh mạch máu
|
Vascular endothelial growth factor (VEGF), angiopoietin
|
|
Ức chế con đường PI3K/AKT/mTOR
|
mTOR, PAN-PI3K, Dual PI3K/mTOR, Dual AKT/ERK
|
|
Ức chế sự sao chép DNA
|
Poly ADP ribose polymerase (PARP)
|
|
Kích hoạt con đường tín hiệu Wnt
|
DKK1
|
|
Ức chế tyrosine kinase (TKI)
|
VEGFR, FGFR, PDGFR, KIT, FLT3, HER2, HER3
|
|
Điều hòa chu trình tế bào, sự sinh sôi và sự sống sót của tế bào
|
CDK4/6/9, PLK1, MEK ½, FR, TROP-2, DHFR, activin A
|
Ghi chú: ICI (immune checkpoint inhibitor): chất ức chế điểm kiểm sóa miễn dịch; EC (endometrial cancer: ung thư nội mạc tử cung; TKI (tyrosine kinase inhibitor): chất ức chế tyrosine kinase; FR (folate receptor): thụ thể folate; yếu tố phát triển nội mạc mạch máu (vascular endothelial growth factor: VEGF), có nguồn gốc từ yếu tố thấm mạch máu (vascular permeability factor: VPF), là một protein tín hiệu (signal protein) được sản xuất bởi nhiều loại tế bào, có khả năng kích thích sự hình thành các mạch máu; antiangiogenesis: chống sự hình thành các mạch máu.
5.2. Các điều trị đích ung thư nội mạc tử cung
Các điều trị đích (targeted therapies) hay còn gọi là các điều trị đích phân tử (molecular-targeted therapies: MTTs) là việc sử dụng các loại thuốc được thiết kế để nhắm đích vào những phân tử (gen hoặc protein) bị thay đổi trong tế bào ung thư. Nói chung, các thuốc điều trị đích có các tác dụng phụ ít nghiêm trọng hơn so với hóa trị liệu (chemotherapy).
Đến nay chỉ có một số thuốc điều trị ung thư nội mạc tử cung được sử dụng như một phần của thử nghiệm lâm sàng, trong khi nhiều loại khác còn đang được nghiên cứu. Các thuốc điều trị đích có thể được sử dụng để điều trị các ung thư nội mạc tử cung có nguy cơ cao và những ung thư đã di căn (metastasized) hoặc tái phát (recurred) sau điều trị, gồm:
5.2.1. Các chất ức chế kinase (kinase inhibitors)
Lenvatinib (Lenvima) là một loại thuốc được biết đến như một chất ức chế kinase (kinase inhibitor). Lenvatinib giúp ngăn chặn các khối u hình thành các mạch máu mới, cũng như nhắm đích vào một số protein trong tế bào ung thư vốn thường giúp khối u phát triển. Lenvatinib có thể được sử dụng cùng với một thuốc điều trị miễn dịch là kháng thể đơn dòng (monocolonal antibody) có tên là pembrolizumab (Keytruda) để điều trị ung thư nội mạc tử cung tiến triển, thường là sau khi đã thử ít nhất một phương pháp điều trị bằng thuốc khác. Lenvatinib được dùng dưới dạng viên nang mỗi ngày một lần.
Makker V và cộng sự, 2022 [8] đã nghiên cứu về điều trị đích trên tổng số 827 bệnh nhân, trong đó 697 bệnh nhân có sự sửa chữa ghép cặp DNA không phù hợp (mismatch repair-proficient disease: pMMR) và 130 bệnh nhân không có sự sửa chữa ghép cặp DNA không phù hợp được chỉ định ngẫu nhiên để nhận lenvatinib cộng với pembrolizumab (411 bệnh nhân) hoặc hóa trị liệu (416 bệnh nhân). Thời gian sống thêm với u không tiến triển trung bình với lenvatinib cộng với pembrolizumab dài hơn so với hóa trị liệu (số bệnh nhân pMMR: 6,6 so với 3,8 tháng; tỷ lệ nguy cơ tiến triển hoặc tử vong là 0,60; khoảng tin cậy [CI] 95%, 0,50 đến 0,72; P<0,001; tổng thể: 7,2 so với 3,8 tháng; tỷ lệ nguy cơ là 0,56; [CI] 95%, 0,47 đến 0,66; P<0,001). Thời gian sống thêm trung bình tổng thể với lenvatinib cộng với pembrolizumab dài hơn so với hóa trị liệu (số bệnh nhân pMMR: 17,4 so với 12,0 tháng; tỷ lệ nguy cơ tử vong là 0,68 ([CI] 95%, 0,56 đến 0,84); P<0,001). Như vậy, ở những bệnh nhân ung thư nội mạc tử cung tiến triển, sự điều trị kết hợp lenvatinib với pembrolizumab dẫn đến thời gian sống thêm với u không tiến triển và thời gian sống thêm tổng thể đều dài hơn một cách có ý nghĩa rất rõ rệt.
Sự kết hợp lenvatinib với pembrolizumab đã được FDA phê chuẩn 21/7/2021 để điều trị đích ung thư biểu mô nội mạc tử cung tiến triển (advanced endometrial carcinoma) không có sự mất ổn định vi ghép cặp DNA không phù hợp cao (microsatellite instability-high: MSI-H) hoặc suy giảm ghép cặp DNA không phù hợp (mismatch repair deficiency of DNA: dMMR).
5.2.2. Các chất ức chế sự hình thành các mạch máu (angiogenesis inhibitors)
Sự hình thành các mạch máu mới là rất quan trọng đối với sự phát triển và di căn của ung thư, trong đó có ung thư nội mạc tử cung. Yếu tố tăng trưởng nội mô mạch máu (vascular endothelial growth factor: VEGF) kích hoạt sự hình thành các mạch máu mới và trở thành đích cho các thuốc ức chế sự hình thành mạch máu. Sự biểu hiện của yếu tố tăng trưởng nội mô mạch máu (VEGF) được thấy ở phần lớn (56% đến 100%) các mẫu ung thư nội mạc tử cung.
Bevacizumab (Avastin) cũng là một kháng thể đơn dòng thuộc nhóm các chất ức chế sự hình thành các mạch máu (angiogenesis inhibitors). Để ung thư phát triển và lây lan, khối u cần hình thành các mạch máu mới để nuôi dưỡng chúng. Bevacizumab gắn vào một protein tên là yếu tố tăng trưởng nội mô mạch máu (vascular endothelial growth factor: VEGF) để làm chậm hoặc ngừng sự phát triển của ung thư. Bevacizumab thường được dùng cùng với thuốc hóa trị liệu, cũng có thể được dùng một mình, thường là sau khi đã thử điều trị bằng các thuốc khác. Bevacizumab được truyền vào tĩnh mạch (IV) sau 2 đến 3 tuần/một lần.
5.2.3. Các chất ức chế mTOR (mTOR inhibitors)
Trong số các điều trị đích được nghiên cứu trong điều trị ung thư nội mạc tử cung, các chất ức chế con đường tín hiệu phân tử (molecular signaling pathways) PI3K/AKT/mTOR được chú ý nhiều nhất. Con đường tín hiệu PI3K/AKT/mTOR được kích hoạt thường xuyên nhất trong ung thư nội mạc tử cung, thúc đẩy tăng trưởng tế bào (cellular growth), chuyển hóa (metabolism), tăng sinh (proliferation), sự sống sót (survival), di cư (migration), sự chết tế bào theo chương trình (apoptosis) và sự hình thành mạch máu (angiogenesis). Ngoài ra, 93% ung thư nội mạc tử cung có các đột biến trên con đường này, cho thấy có khả năng áp dụng các chất ức chế con đường PI3K/AKT/mTOR là một điều trị đích. Các chất đại diện cho các chất ức chế con đường tín hiệu này bao gồm các chất ức chế mTOR (ridaforolimus, everolimus, temsirolimus), các chất ức chế PI3K (PI3K inhibitors) (BKM120, Pilaralisib, PF-04691502 và PF-05212384), chất ức chế kép PI3K/mTOR (GDC-0980) và chất ức chế AKT (MK-2206). Tuy nhiên, việc điều trị bằng các chất ức chế con đường PI3K/AKT/mTOR đơn lẻ chỉ cho tác dụng khiêm tốn với tỷ lệ đáp ứng (OR) hoàn toàn và đáp ứng một phần là <10% ở các thử nghiệm pha 2 trong điều trị EC tái phát và di căn, trừ temsirolimus có tỷ lệ OR là 22%. Các chất ức chế mTOR có tác dụng ngăn chặn một protein tế bào là mTOR, là loại protein có tác dụng giúp tế bào phát triển và phân chia thành các tế bào mới. Các chất ức chế mTOR có thể được sử dụng một mình hoặc kết hợp với thuốc hóa trị liệu hoặc điều trị hormon để điều trị ung thư nội mạc tử cung tiến triển hoặc tái phát sau khi điều trị. Các chất ức chế mTOR có thể gồm:
1) Everolimus (Afinitor) là một thuốc ức chế mTOR được dùng dưới dạng viên uống mỗi ngày một lần. Các tác dụng phụ có thể gặp của everolimus gồm lở miệng, tiêu chảy, buồn nôn, cảm thấy yếu hoặc mệt mỏi, khó thở và ho. Everolimus cũng có thể gây ra công thức máu thấp, tăng lipid máu (cholesterol và triglyceride) và tăng lượng đường trong máu, vì vậy cần xét nghiệm máu thường xuyên khi sử dụng loại thuốc này.
2) Temsirolimus (Torisel) là một thuốc ức chế mTOR khác được sử dụng dưới dạng tiêm tĩnh mạch (IV), thường một lần một tuần. Temsirolimus có thể được sử dụng một mình.
5.2.4. Các chất mới nổi khác (other emerging agents)
Hiện tại, nhiều chất nhắm đích mới nổi khác đang được xem là phương pháp điều trị tiềm năng cho ung thư nội mạc tử cung và danh sách này đang phát triển nhanh khi chúng ta ngày càng hiểu rõ hơn về cơ sở phân tử cơ bản của ung thư nội mạc tử cung loại I và II cũng như bốn kiểu phụ của ung thư nội mạc tử cung. Các chất ức chế PARP (poly [ADP]-ribose polymerase inhibitors) tác động lên con đường tín hiệu mTOR, làm PTEN mất chức năng, dẫn đến suy giảm khả năng tái tổ hợp tương đồng của các đứt gãy sợi kép DNA. Do có sự quan hệ giữa sự mất PTEN và sự ức chế PARP, các chất ức chế PARP có thể được sử dụng đơn lẻ hoặc kết hợp với các chất ức chế mTORC1/2 và chất ức chế AKT trong điều trị ung thư nội mạc tử cung.
Phần lớn các ung thư nội mạc tử cung có sự biểu hiện của protein chết tế bào theo chương trình PD-1 (PD1 programmed death protein). Ngoài ra, các ung thư nội mạc tử cung có các gen POLE (polymerase ε) và MSI (microsatellite instability: không ổn định vi ghép cặp DNA) có số lượng đột biến cao cũng có biểu hiện PD-1 cao. Việc điều trị ung thư nội mạc tử cung bằng pembrolizumab - một chất ức chế điểm kiểm soát miễn dịch chống PD-1 (an anti-PD-1 immune checkpoint inhibitor) hiện đang được thử nghiệm giai đoạn 2.
Béo phì, đái tháo đường và sự kháng insulin có liên quan đến việc tăng nguy cơ và kết quả kém hơn đối với ung thư nội mạc tử cung. Metformin là một biguanide thường được sử dụng đầu tay để điều trị đái tháo đường loại 2. Bằng chứng cho thấy việc sử dụng metformin có thể làm giảm nguy cơ ung thư và làm giảm tử vong do ung thư ở bệnh nhân đái tháo đường, trong đó có ung thư nội mạc tử cung. Metformin được cho là có tác dụng chống khối u thông qua tác dụng gián tiếp làm giảm nồng độ glucose máu và tác động trực tiếp lên khối u thông qua việc ức chế phức hợp ty thể 1, kích hoạt gen AMPK và ức chế con đường mTOR. Hiện nay, một số thử nghiệm lâm sàng giai đoạn II của metformin trong điều trị ung thư nội mạc tử cung tiến triển đang được thực hiện, chẳng hạn như sự kết hợp metformin với levonorgestrel, sự kết hợp metformin với letrozole, của mirena một mình hoặc kết hợp với metformin, của megestrol acetate một mình hoặc kết hợp với metformin và của sự kết hợp của ba thuốc gồm cyclophosphamide, metformin và olaparib [1, 2, 7, 10].
Tóm lại, các yếu tố nguy cơ của ung thư nội mạc tử cung có thể liên quan đến sự tiếp xúc quá mức của nội mạc tử cung với estrogen, bao gồm liệu pháp estrogen không bị đối kháng, có sớm, mãn kinh muộn, điều trị tamoxifen, chưa sinh đẻ, vô sinh hoặc không rụng trứng và hội chứng buồng trứng đa nang. Các yếu tố nguy cơ khác là tuổi tăng, béo phì, tăng huyết áp, đái tháo đường và ung thư đại trực tràng không đa polyp di truyền. Các dấu hiệu và triệu chứng của ung thư nội mạc tử cung có thể bao gồm chảy máu âm đạo sau khi mãn kinh, chảy máu giữa các kỳ kinh và đau vùng chậu. Các dấu ấn sinh học khối u huyết thanh đối với ung thư nội mạc tử cung bao gồm: CA125 là dấu ấn khối u chính trong chẩn đoán, theo dõi và tiên lượng ung thư nội mạc tử cung; HE4 có tiềm năng tốt hơn CA125 trong chẩn đoán ung thư nội mạc tử cung; sự kết hợp của CA125 và HE4 tốt hơn từng dấu ấn đơn lẻ. Các dấu ấn sinh học dựa trên sinh thiết lỏng đối với ung thư nội mạc tử cung bao gồm các tế bào khối u lưu thông (CTCs), các DNA khối u lưu thông (ctDNAs), RNA không mã hóa dài (lncRNA), microRNA (miNA), các vi túi (cMVs), các tiểu cầu nuôi khối u (TEPs), mRNA (mRNA) và protein có thể đóng các vai trò khác nhau trong chẩn đoán, tiên lượng và quản lý bệnh nhân. Các con đường tín hiệu phân tử chính của ung thư nội mạc tử cung bao gồm con đường tín hiệu RTK, con đường tín hiệu Wnt, con đường tín hiệu Notch, con đường tín hiệu p53 và p16. Các điều trị đích ung thư nội mạc tử cung bao gồm: Các chất ức chế thụ thể yếu tố tăng trưởng biểu bì (EGFR) kinase; các chất ức chế sự hình thành mạch máu; các chất ức chế mTOR, và các thử nghiệm lâm sàng giai đoạn 2 đang diễn ra bao gồm các chất ức chế điểm kiểm soát miễn dịch và các thuốc ức chế poly (ADP-ribose) polymerase (PARP).
Tài liệu tham khảo
1. ACS. Targeted Therapy for Endometrial Cancer, American Cancer Society, 2019.
2. Barretina-Ginesta MP, Quindós M, Alarcón JD, et al. SEOM-GEICO clinical guidelines on endometrial cancer. Clin Transl Oncol 2022; 24(4): 625-634.
3. Bidzinski M, Danska-Bidzinska A, Rychlik A, et al. Molecular classification of endometrial carcinoma, is it the new era of precision medicine? Ginekol Pol 2022; 93(2):163-167.
4. Coada CA, Dondi G, Ravegnini G, et al. Classification Systems of Endometrial Cancer: A Comparative Study about Old and New. Diagnostics (Basel) 2022 Jan; 12(1): 33.
5. Cymbaluk-Płoska A, Gargulińska P, Bulsa M, Kwiatkowski S Chudecka-Głaz A, and Michalczyk K. Can the Determination of HE4 and CA125 Markers Affect the Treatment of Patients with Endometrial Cancer? Diagnostics (Basel) 2021 Apr; 11(4): 626.
6. Dong C, Liu P and Li C. Value of HE4 Combined with Cancer Antigen 125 in the Diagnosis of Endometrial Cancer. Pak J Med Sci 2017 Jul-Aug; 33(4): 1013-1017.
7. Lee SY. Tailored Therapy Based on Molecular Characteristics in Endometrial Cancer. Biomed Res Int 2021; 2021: 2068023.
8. Makker V, Colombo N, Herráez AC, et al. Lenvatinib plus Pembrolizumab for Advanced Endometrial Cancer. N Engl J Med 2022 Feb 3; 386(5): 437-448.
9. Malentacchi F, Sgromo C, Antonuzzo L, and Pillozzi S. Liquid biopsy in endometrial cancer. J Cancer Metas Treat 2020; 6: 1-20.
10. Mitamura T, Dong P, Ihira K, Kudo M, and Watari H. Molecular-targeted therapies and precision medicine for endometrial cancer. Jpn J Clin Oncol 2019 Feb 1; 49(2): 108-120.
11. Muinelo-Romay L, Casas-Arozamena C, and Abal M. Liquid Biopsy in Endometrial Cancer: New Opportunities for Personalized Oncology. Int J Mol Sci 2018 Aug; 19(8): 2311.
12. Rajadevan N, McNally O, Neesham D, Richards A, and Naaman Y. Prognostic value of serum HE4 level in the management of endometrial cancer: A pilot study. Aust N Z J Obstet Gynaecol 2021 Apr; 61(2): 284-289.
13. Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, and Bray F. Global cancer statistics 2020: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA A Cancer J Clin 2021; 71: 209-249.
14. Urick ME, Bell DW. Clinical actionability of molecular targets in endometrial cancer. Nat Rev Cancer 2019; 19(9): 510-521.
15. Yen TT, Wang TL, Fader AN, Shih IM, and Gaillard S. Molecular Classification and Emerging Targeted Therapy in Endometrial Cancer. Int J Gynecol Pathol 2020 Jan; 39(1): 26-35.
16. Wang Y, Han C, Teng F, Bai Z, Tian W, and Xue F. Predictive value of serum HE4 and CA125 concentrations for lymphatic metastasis of endometrial cancer. Int J Gynaecol Obstet 2017 Jan; 136(1): 58-63.


