NSE là tên viết tắt của enzyme enolase đặc hiệu thần kinh (neuron specific enolase), là một dấu ấn ung thư có bản chất enzyme, đặc hiệu cho ung thư phổi tế bào nhỏ (small cell lung cancer: SCLC) và u nguyên bào thần kinh (neuroblastoma).
21/06/2019 | Chụp cắt lớp phổi và những lưu ý quan trọng trước khi thực hiện 02/06/2019 | Chụp X - quang phổi có thể phát hiện bệnh gì? 31/05/2019 | Hút thuốc lá - Nguyên nhân hàng đầu gây ung thư phổi
Ung thư phổi hiện là loại ung thư hay gặp nhất trên thể giới, với số ca mới được chẩn đoán trong năm 2012 là 1.825.000 ca, chiếm 13% trong tổng số các ung thư. Trong số đó, ung thư phổi tế bào nhỏ chiếm 10-15% (WHO, 2012).
U nguyên bào thần kinh là một loại ung thư bắt nguồn từ các tế bào thần kinh, hay gặp ở trẻ dưới 5 tuổi, hiếm khi gặp ở trẻ trên 10 tuổi, thường khu trú ở quanh tuyến thượng thận, cũng có thể gặp ở vùng cổ, ngực, bụng và vùng hố chậu. U nguyên bào thần kinh chiếm 7% trong tổng số ung thư ở trẻ em nhưng gây nên trên 10% số tử vong do ung thư ở trẻ em.
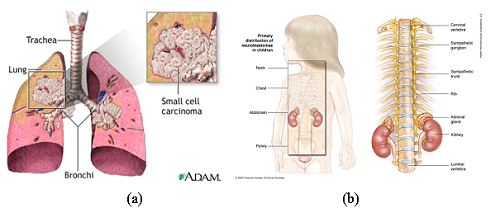
Hình 1. (a) Hình ảnh ung thư phổi tế bào nhỏ và (b) các vị trí u nguyên bào thần kinh
1. Sinh học của NSE
NSE (neuron-specific enolase hay γ-enolase) là một isoenzyme của enzyme enolase (EC 4.2.1.11). Enolase là một trong 11 enzyme của con đường đường phân glucose, một enzyme đồng phân hóa, xúc tác cho phản ứng biến 2-phosphoglycerate thành phosphoenolpyruvate. Enolase có dạng dimer, do 2 trong số 3 tiểu đơn vị (subunit) α, β và γ, mỗi tiểu đơn vị có khối lượng phân tử 39 kDa, có các tính chất miễn dịch, hóa sinh và đặc hiệu cơ quan khác nhau, kết hợp với nhau tạo thành. Các tiểu đơn vị này có 5 khả năng kết hợp khác nhau: αα, ββ, γγ, αγ và αβ và mỗi loại được tổng hợp bởi các loại tế bào khác nhau. NSE là loại enzyme γ-enolase dimer, do 2 chuỗi γ hoặc do 1 chuỗi α và 1 chuỗi γ kết hợp với nhau tạo thành (dạng γγ hoặc αγ) (Qi W 2014 [5]). Thời gian bán hủy (half-life) của NSE trong các dịch của cơ thể là khoảng 24 giờ.
NSE huyết thanh hoặc huyết tương được định lượng bằng phương pháp miễn dịch điện hóa phát quang (electro-chemiluminescence immunoassay: ECLIA) trên máy phân tích miễn dịch Elecsys-Cobas e*.
Xét nghiệm NSE được sử dụng để chẩn đoán, đánh giá giai đoạn bệnh và theo dõi hiệu quả điều trị ở các bệnh nhân có khối u thần kinh nội tiết (neuroendocrine tumors), đặc biệt là ung thư phổi tế bào nhỏ (small cell lung cancer) và u nguyên bào thần kinh (neuroblastoma).
Xét nghiệm này không phù hợp để sàng lọc trong cộng đồng không có triệu chứng với mục đích phát hiện ung thư phổi tế bào nhỏ bởi vì độ nhạy và độ đặc hiệu lâm sàng của nó thấp.
3. Chỉ định của xét nghiệm NSE
- Chẩn đoán, chẩn đoán phân biệt, theo dõi hiệu quả điều trị, phát hiện tái phát và tiên lượng ở bệnh nhân ung thư phổi tế bào nhỏ.
- Chẩn đoán, theo dõi hiệu quả điều trị, phát hiện tái phát và tiên lượng ở bệnh nhân u nguyên bào thần kinh.
4. Giá trị tham chiếu của NSE
Ở người lớn: Mức độ NSE huyết thanh người bình thường là ≤ 15 ng/mL.
Ở trẻ em: Mức độ NSE huyết thanh trẻ em < 1 tuổi là ≤ 25 ng/mL; Mức độ NSE huyết thanh trẻ em 1-5 tuổi là ≤ 20 ng/mL; Mức độ NSE huyết thanh trẻ em 6-8 tuổi là ≤ 18 ng/mL; Mức độ NSE dịch não tủy người bình thường là 0-3,7 ng/mL.
5. Ý nghĩa lâm sàng
5.1. NSE trong ung thư phổi tế bào nhỏ
Ngay từ những năm 1980, người ta đã phát hiện ra rằng mức độ CEA huyết thanh tăng trong ung thư phổi tế bào nhỏ. Mức độ NSE huyết thanh tăng >25 ng/mL được phát hiện ở 72% các trường hợp ung thư phổi tế bào nhỏ trong khi chỉ tăng ở khoảng 8% trong các thể ung thư phổi khác. Vì vậy, NSE được xem như là dấu ấn được lựa chọn đầu tiên trong theo dõi ung thư phổi tế bào nhỏ và nó có giá trị trong chẩn đoán, tiên lượng, theo dõi hiệu quả điều trị và phát hiện tái phát sau điều trị của những bệnh nhân này.
Độ nhạy chẩn đoán của NSE huyết thanh ở bệnh nhân ung thư phổi tế bào nhỏ tăng theo mức độ bệnh. Trong một nghiên cứu, Poposka BI, 2004 [4] đã chỉ ra rằng, với giá trị cắt (cut-off) >16,6 ng/mL, ở giai đoạn bệnh khu trú (limited disease: LD), độ nhạy của NSE là 55,5%, trong khi ở giai đoạn bệnh di căn (extensive disease: ED) độ nhạy của NSE có thể lên đến 100% (Bảng 1).
Bảng 1. Giá trị trung bình và độ nhạy của NSE huyết thanh với giá trị cắt 16,6 ng/mL ở bệnh nhân ung thư phổi tế bào nhỏ theo giai đoạn (Poposka BI, 2004 [4]
|
Nhóm
|
NSE (ng/mL)
|
Tỷ lệ giá trị NSE tăng >16,6 ng/mL
|
Độ nhạy
|
|
Người bình thường
|
8,01 ± 4,40
|
|
|
|
SCLC khu trú
|
46,94 ± 56,92
|
10/18
|
55,5%
|
|
SCLC di căn
|
290,48 ± 325,24
|
15/15
|
100%
|
Độ nhạy của NSE huyết thanh của bệnh nhân ung thư phổi tế bào nhỏ với các giá trị cắt khác nhau ở mức độ còn khu trú và đã di căn đã được Monila M, 2005 [3] chỉ ra ở Bảng 2.
Bảng 2. Độ nhạy của NSE huyết thanh ở các giá trị cắt khác nhau ở bệnh nhân ung thư phổi tế bào nhỏ (Monila M, 2005 [3]).
|
Các giá trị cắt của NSE (ng/mL)
|
Độ nhạy của NSE huyết thanh (%)
|
|
Chung
|
SCLC khu trú
|
SCLC di căn
|
|
NSE >20
|
64
|
46
|
73
|
|
NSE >30
|
74,4
|
61,5
|
80
|
|
NSE >35
|
90
|
75
|
96
|
|
NSE >40
|
100
|
100
|
100
|
Khi so sánh độ nhạy của một số dấu ấn ung thư phổi, trong một nghiên cứu của Wojcik 2008 [7], ở bệnh nhân ung thư phổi tế bào nhỏ, mức độ tăng của ProGRP, NSE và CYFRA 21-1 trước điều trị được thấy tương ứng là 79,7%, 57,8% và 23,4%. Trong một nghiên cứu khác, Monila M, 2005 [3] thấy rằng, mức độ các dấu ấn ung thư ProGRP, NSE, CEA, CYFRA 21-1 và SCC huyết tương tăng trong ung thư phổi tế bào nhỏ tương ứng là 73%, 64%, 53%, 46% và 4,5%, trong khi ở ung thư tế bào không nhỏ (non-small cell lung cancer: NSCLC), mức độ của các dấu ấn này chỉ tăng tương ứng là 30%, 22,5%, 55,6%, 65,2% và 26,7%.
Về sự kết hợp giữa các dấu ấn ung thư, sự kết hợp dấu ấn ung thư tốt nhất trong ung thư phổi tế bào nhỏ là NSE và ProGRP với độ nhạy là 88%, còn trong ung thư phổi tế bào không nhỏ, sự kết hợp dấu ấn ung thư tốt nhất lại là CYRA 21-1 và CEA với độ nhạy là 82%. Một số tác giả cũng cho rằng, trong ung thư phổi tế bào nhỏ, sự kết hợp NSE với ProGRP có thể làm tăng độ nhạy chẩn đoán thêm từ 14% đến 23%, còn nếu bổ sung thêm hai xét nghiệm nữa là CYFRA 21-1 và CEA thì cũng không làm độ nhạy chẩn đoán tăng thêm. Mao CY, 2015 [2] cũng chỉ ra rằng độ nhạy và độ đặc hiệu của sự kết hợp NSE và ProGRP trong chẩn đoán ung thư phổi tế bào nhỏ tương ứng là 88% và 81%, còn độ chính xác (diện tích dưới đường cong ROC) là 93,79 ± 1,08%.
Về mức độ tăng của NSE theo mức độ bệnh, sự tăng NSE có liên quan đến giai đoạn lâm sàng. Trong nghiên cứu của Monila M, 2005 [2], khi ung thư phổi tế bào nhỏ còn chưa xâm lấn, mức độ tăng của NSE gặp ở 80,7% số bệnh nhân, trong khi ở giai đoạn khối u lan tỏa, mức độ tăng của NSE tăng đến 90,2% số bệnh nhân. Tuy nhiên, sự tăng NSE huyết tương không liên quan với vị trí di căn của ung thư phổi tế bào nhỏ.
Xét nghiệm NSE cũng có giá trị trong theo dõi đáp ứng điều trị ung thư phổi tế bào nhỏ. Nếu hóa trị liệu thành công, mức độ NSE trong huyết tương có thể tăng tạm thời trong 24-72 giờ do sự phân hủy tế bào khối u, sau đó sẽ nhanh chóng giảm xuống với chu kỳ bán hủy khoảng 24 giờ. Khi ung thư tái phát, mức độ NSE huyết thanh lại tăng lên. Sự thay đổi mức độ NSE huyết thanh (ng/mL) trong quá trình điều trị ở các bệnh nhân ung thư phổi tế bào nhỏ (SCLC) là rõ rệt, trong khi sự thay đổi NSE ở ung thư phổi tế bào không nhỏ (NSCLC) là không rõ rệt (Hình 2).
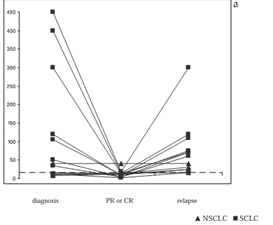
Hình 2. Những thay đổi về mức độ NSE huyết thanh (ng/mL) (trục tung) ở bệnh nhân ■: ung thư phổi tế bào nhỏ (SCLC) và ▲: ung thư phổi tế bào không nhỏ (NSCLC) trong quá trình điều trị. Trục hoành: thời điểm diagnosis là chẩn đoán; PR là đáp ứng một phần (partial respnonse) hoặc CR là đáp ứng hoàn toàn (complete response); relapse là tái phát.
Về giá trị tiên lượng bệnh, NSE trước điều trị là một yếu tố tiên lượng ở bệnh nhân ung thư phổi tế bào nhỏ giai đoạn khối u còn khu trú tốt hơn ProGRP, tuy nhiên, sau điều trị, cả hai dấu ấn này có giá trị tiên lượng tương tự như nhau (Wojcik E, 2007 [7]). Tổng kết 11 nghiên cứu được công bố với tổng số 3.397 bệnh nhân ung thư phổi tế bào nhỏ và 3.344 người đối chứng khỏe mạnh, Zhao WX và Luo JF, 2013 [9] thấy rằng có khoảng 68,6% số bệnh nhân có mức độ NSE huyết thanh tăng so với các giá trị cắt được các tác giả đưa ra. Tỷ lệ nguy cơ (hazard ratio: HR) của mức độ NSE huyết thanh cao đối với sự sống còn (overall survival: OS) ở bệnh nhân ung thư phổi tế bào nhỏ là 1,74 lần so với mức độ NSE huyết thanh thấp. Trong ung thư phổi tế bào nhỏ, với mức độ NSE huyết thanh <25 ng/mL, thời gian sống sót trung bình của bệnh nhân là 15 tháng và tỷ lệ sống 2 năm là 27%, trong khi với mức độ NSE huyết thanh >25 ng/mL, thời gian sống sót trung bình chỉ là 7,5 tháng và tỷ lệ sống 2 năm chỉ còn 1%.
Ung thư phổi có thể phòng tránh được nếu được phát hiện sớm và điều trị kịp thời.
5.2. Xét nghiệm NSE trong u nguyên bào thần kinh ở trẻ em
Trong một nghiên cứu, Bolkar ST và cộng sự, 2008 [1] đã chỉ ra rằng ở các bệnh nhi bị u nguyên bào thần kinh, mức độ NSE huyết thanh tăng lên một cách có ý nghĩa so với nhóm đối chứng bình thường: NSE = 60,84 ± 47,28 ng/mL so với 6,2 ± 3,5 ng/mL ( p<0,001). Trong u nguyên bào thần kinh, cùng với sự tăng NSE, một số dấu ấn sinh học khác như Ferritin, LDH (lactate dehydrogenase) trong huyết thanh và VMA (Vanillyn Mandellic Acid) trong nước tiểu cũng tăng một cách có ý nghĩa.
Về vai trò của NSE trong u nguyên bào thần kinh, Singal AK và Agarwala S, 2005 [6] cho rằng:
- Xét nghiệm NSE có đủ độ nhạy để chẩn đoán u nguyên bào thần kinh nhưng do mức độ NSE cũng có thể tăng trong một số các khối u thần kinh khác như u tế bào ưa chrom (pheochromocytoma), ung thư biểu mô tuyến giáp thể tủy, ung thư tế bào đảo tụy và các u tế bào thần kinh nội tiết (carcinoids), … nên NSE có độ đặc hiệu thấp.
- Mức độ NSE huyết thanh có sự tương quan với khối lượng khối u và tiên lượng bệnh: mức độ NSE >100 ng/mL tại thời điểm chẩn đoán tương quan với độ lớn của khối u và chỉ ra một tiên lượng kém, trong khi mức độ NSE <30 ng/mL cho phép dự đoán một đáp ứng điều trị tốt.
- Không có sự khác nhau về mức độ NSE khi u nguyên bào thần kinh khu trú ở nhưng vị trí khác nhau trong cơ thể.
- Việc xét nghiệm một loạt NSE theo thời gian cho phép theo dõi đáp ứng đối với hóa trị liệu: mức độ tăng sau điều trị có nghĩa là u tái phát.
5.3. NSE trong một số bệnh lành tính
- Mức độ NSE huyết thanh có thể tăng ở 5% (với mức độ > 12 ng/mL) số các bệnh phổi lành tính.
- Trong các bệnh não, mức độ NSE có thể tăng trong dịch não tủy ở các bệnh nhân bị viêm màng não - mạch máu não (serebrovasculer meningitis), viêm não rải rác (disseminated encephalitis), thoái hóa tủy sống - tiểu não (spinocerebellar degeneration), thiếu máu cục bộ và tắc mạch não (cerebral ischemia and infraction), nhồi máu não (intracerebral hematomas), chảy máu dưới màng nhện (subarachnoid hemorrhages), viêm não, …
- Ngoài ra, mức độ NSE cũng có thể tăng trong thiếu máu tan huyết vì trong hồng cầu có NSE, suy gan và suy thận giai đoạn cuối, …, hoặc khi điều trị với thuốc ức chế bơm proton.
Kết luận
1. NSE là một dấu ấn ung thư loại protein enzyme có nguồn gốc từ các tế bào thần kinh.
2. NSE có thể được chỉ định để chẩn đoán, chẩn đoán phân biệt, theo dõi hiệu quả điều trị, phát hiện tái phát và tiên lượng ở bệnh nhân ung thư phổi tế bào nhỏ hoặc u nguyên bào thần kinh.
3. Các kết quả nghiên cứu đã chứng minh rằng NSE huyết thanh là một dấu ấn có giá trị để chẩn đoán, đánh giá giai đoạn bệnh, theo dõi đáp ứng điều trị, phát hiện tái phát và tiên lượng ở bệnh nhân ung thư phổi tế bào nhỏ.
4. Sự kết hợp NSE với ProGRP làm tăng độ nhạy trong chẩn đoán ung thư phổi tế bào nhỏ và sự kết hợp này có thể là một chỉ dẫn quan trọng cho chẩn đoán sớm ung thư phổi tế bào nhỏ.
5. Trong u nguyên bào thần kinh ở trẻ em, NSE huyết thanh có thể được sử dụng để chẩn đoán, đánh giá khối lượng khối u và tiên lượng bệnh.
Tài liệu tham khảo
1. Bolkar ST, Ghadge MS and Raste AS. Biochemical parameters in neuroblastoma. Indian Journal of clinical Biochemistry 2008; 23(3): 293-295.
2. Mao CY, Kai XU, Lai YY, and Liu LL. Systematic review of value of combined detection of ProGRP/NSE in diagnosis of small cell lung cancer patients. Clinical Research 2015, 15(4): 452-456.
3. Molina R, Auge JM, Filella X, et al. Pro-gastrin-releasing peptide (proGRP) in patients with benign and malignant diseases: comparison with CEA, SCC, CYFRA 21-1 and NSE in patients with lung cancer. Anticancer Res 2005 May-Jun; 25(3A): 1773-1778.
4. Poposka BI, Spirovski M, Trajkov D, et al. Neuro specific enolase – selective marker for small cell lung cancer. Radiol Oncol 2004; 38(1): 21-26.
5. Qi W, Li X, Kang J. Advances in the study of serum tumor markers of lung cancer. J Can Res Ther 2014; 10: 95 -101.
6. Singal AK, Agarwala. Tumour markers in pediatric solid tumour. J Indian Assoc Pediatr Surg 2005 Jul-Sept; 10(3): 183-190.
7. Wójcik E, Kulpa JK, Sas-Korczynska B, Korzeniowski S, Jakubowicz J. ProGRP and NSE in therapy monitoring in patients with small cell lung cancer. Anticancer Res 2008 Sep-Oct; 28(5B): 3027-3033.
8. Wojcik E, Kulpa JK, Sas-Korczynska B. ProGRP and NSE for follow-up of small cell lung cancer patients with limited disease: P2-061. J Thoracic Oncol 2007; 2(8): S514.
9. Zhao WX, Luo JF. Serum neuron-specific enolase levels were associated with the prognosis of small cell lung cancer: a meta-analysis. Tumour Biol 2013 Oct; 34(5): 3245-3248.
*Hiện nay, mức độ NSE huyết thanh định lượng bằng phương pháp miễn dịch điện hóa phát quang trên máy phân tích miễn dịch Elecsys-Cobas e, đang được thực hiện hàng ngày tại Bệnh viện Đa khoa MEDLATEC 42 Nghĩa Dũng, Ba Đình, Hà Nội.


